검색결과
-
![[영국] 특허청(IPO), 표준 필수 특허(SEP) 관련 의견에 대한 답변 요약본 출판](http://www.stdnews.kr/data/file/news/thumb/thumb-1794764642_e0oljGvZ_0c4050a0e706568f2fe4af2a1c1d9a6ef7fe77f2_200x180.jpg) [영국] 특허청(IPO), 표준 필수 특허(SEP) 관련 의견에 대한 답변 요약본 출판영국 특허청(Intellectual Property Office, IPO)에 따르면 2022년 8월 5일 표준 필수 특허(standard essential patent, SEP) 관련 의견에 대한 답변을 정리한 요약본을 출판했다.표준 필수 특허(SEP)는 표준 구현에 필수적인 기술을 보호하는 특허를 말한다. 표준과 특허는 여러 분야 및 부분에 걸쳐 적용될 수 있다.예를 들면 다른 제조업체의 제품이 소비자에게 기능을 제공하기 위해 상호 원활하게 통신할 수 있어야 한다. 제조자(또는 표준 구현자)가 스마트폰이나 태블릿과 같은 표준 호환 제품을 제조하기 위해서는 SEP에 의해 보호되는 방법이나 장치를 사용하지 않을 경우 불가능하다.특히 통신, 자동차 산업, 사물인터넷(IoT) 분야를 중심으로 3G, 4G, 5G 등 무선 기술 사용이 증가하면서 특허 라이센스와 표준 사용에 대한 관심이 높아지고 있다.따라서 특허청이 실시한 의견 수렴 요청은 산업계가 직면한 과제에 대한 광범위한 견해와 증거를 찾기 위한 것이다.특허청의 의견 요청에 대한 응답은 6가지 주제로 구성돼 있다. 첫째, SEP와 혁신, 경쟁 간의 관계, 영국 내에서 소비자들을 위해 가장 큰 개선을 할 수 있는 행동이나 개입이 무언인가에 관한 것이다.다른 5가지 주제를 세부적으로 살펴 보면 △경쟁과 시장 기능 △제도의 투명성 △특허 침해 및 구제 △SEP의 허가 △SEP 소송 등이다.응답을 받은 증거와 견해는 모든 건에 정부의 개입이 필요한지를 포함해 다음에 어떤 조치를 취할 것인지에 대한 정부의 결정을 알리는데 도움이 될 것이다.정부는 기업들의 우려를 이해하고 있다는 사실을 확인시키기 위해 기업과 지속적으로 협력하고 필요한 경우 추가 증거를 찾는다.조사 결과는 2023년 관련 부처 장관들에게 보고되고 모든 중요 정책 개입은 공개 협의 대상이 된다. 의견 요청은 2021년 12월부터 2022년 3월까지 12주간 진행됐다. 응답자들의 견해 56건을 서면으로 받았다.IPO는 SEP 보유자, 시행자, 법률 및 학술단체, 부분 및 혁신 네트워크 등을 포함한 다양한 이해관계자 그룹과 다수의 원탁회의를 개최했다.공표된 SEP의 수는 1990년대 초부터 2014년까지 5년마다 평균 2배씩 증가했다. 2020년 기준 약 9만5000건의 특허가 5G 표준에 필수적이라고 발표됐다.2019년 말 76억개의 활성 사물인터넷(Internet of Things, IoT) 장치가 보급되면서 관련 분야는 점점 더 중요해지고 있다. 향후 10년간 관련 장치는 대폭 증가할 것으로 예측된다.
[영국] 특허청(IPO), 표준 필수 특허(SEP) 관련 의견에 대한 답변 요약본 출판영국 특허청(Intellectual Property Office, IPO)에 따르면 2022년 8월 5일 표준 필수 특허(standard essential patent, SEP) 관련 의견에 대한 답변을 정리한 요약본을 출판했다.표준 필수 특허(SEP)는 표준 구현에 필수적인 기술을 보호하는 특허를 말한다. 표준과 특허는 여러 분야 및 부분에 걸쳐 적용될 수 있다.예를 들면 다른 제조업체의 제품이 소비자에게 기능을 제공하기 위해 상호 원활하게 통신할 수 있어야 한다. 제조자(또는 표준 구현자)가 스마트폰이나 태블릿과 같은 표준 호환 제품을 제조하기 위해서는 SEP에 의해 보호되는 방법이나 장치를 사용하지 않을 경우 불가능하다.특히 통신, 자동차 산업, 사물인터넷(IoT) 분야를 중심으로 3G, 4G, 5G 등 무선 기술 사용이 증가하면서 특허 라이센스와 표준 사용에 대한 관심이 높아지고 있다.따라서 특허청이 실시한 의견 수렴 요청은 산업계가 직면한 과제에 대한 광범위한 견해와 증거를 찾기 위한 것이다.특허청의 의견 요청에 대한 응답은 6가지 주제로 구성돼 있다. 첫째, SEP와 혁신, 경쟁 간의 관계, 영국 내에서 소비자들을 위해 가장 큰 개선을 할 수 있는 행동이나 개입이 무언인가에 관한 것이다.다른 5가지 주제를 세부적으로 살펴 보면 △경쟁과 시장 기능 △제도의 투명성 △특허 침해 및 구제 △SEP의 허가 △SEP 소송 등이다.응답을 받은 증거와 견해는 모든 건에 정부의 개입이 필요한지를 포함해 다음에 어떤 조치를 취할 것인지에 대한 정부의 결정을 알리는데 도움이 될 것이다.정부는 기업들의 우려를 이해하고 있다는 사실을 확인시키기 위해 기업과 지속적으로 협력하고 필요한 경우 추가 증거를 찾는다.조사 결과는 2023년 관련 부처 장관들에게 보고되고 모든 중요 정책 개입은 공개 협의 대상이 된다. 의견 요청은 2021년 12월부터 2022년 3월까지 12주간 진행됐다. 응답자들의 견해 56건을 서면으로 받았다.IPO는 SEP 보유자, 시행자, 법률 및 학술단체, 부분 및 혁신 네트워크 등을 포함한 다양한 이해관계자 그룹과 다수의 원탁회의를 개최했다.공표된 SEP의 수는 1990년대 초부터 2014년까지 5년마다 평균 2배씩 증가했다. 2020년 기준 약 9만5000건의 특허가 5G 표준에 필수적이라고 발표됐다.2019년 말 76억개의 활성 사물인터넷(Internet of Things, IoT) 장치가 보급되면서 관련 분야는 점점 더 중요해지고 있다. 향후 10년간 관련 장치는 대폭 증가할 것으로 예측된다. -
![[나이지리아] 아프리글로벌 메디케어(Afriglobal Medicare), 6월 ISO 15189:2012 인증 획득](http://www.stdnews.kr/data/file/news/thumb/thumb-988342002_WIuqpCgY_4af9b067cf7f1c11367186e3c2131a7728c5ca42_200x180.jpg) [나이지리아] 아프리글로벌 메디케어(Afriglobal Medicare), 6월 ISO 15189:2012 인증 획득나이지리아 진단 서비스업체인 아프리글로벌 메디케어(Afriglobal Medicare)에 따르면 2022년 6월 ISO 15189:2012 인증을 획득했다.ISO15189:2012는 국제표준화기구(ISO)가 제정한 인증으로 메디컬 시험기관에서 이뤄지는 각종 임상과 관련된 검사가 기술적 요건과 신뢰성을 갖췄다는 것을 보장하는 국제표준이다.인증을 받음으로써 아프리글로벌 메디케어는 국내에서 대단히 필요하고 품질을 갖춘 진단 서비스를 제공하는 장기 전략 여행에 요구되는 필수적인 디딤돌을 마련한 것으로 평가받는다.나이지리아 승인 서비스의 의료연구소과학위원회(Medical Laboratory Science Council)가 표준 인증을 위한 감사 작업을 진행했다. 인증을 받은 핵심 노하우는 2가지로 요약된다.첫째, 베스트 프랙티스에 기반한 운영을 활용하는 글로벌 수준의 시스템을 갖춘 연구소를 건설했다. 둘째, 연구소는 고객과 사회를 위해 최고 수준의 품질 표준을 운영하기 위해 노력했다.참고로 아프리글로벌 메디케어는 매일 3500건 이상의 샘플을 분석해 질병을 진단한다. 코로나19 진단을 포함해 1일 24시간 365일 운영 중이다.
[나이지리아] 아프리글로벌 메디케어(Afriglobal Medicare), 6월 ISO 15189:2012 인증 획득나이지리아 진단 서비스업체인 아프리글로벌 메디케어(Afriglobal Medicare)에 따르면 2022년 6월 ISO 15189:2012 인증을 획득했다.ISO15189:2012는 국제표준화기구(ISO)가 제정한 인증으로 메디컬 시험기관에서 이뤄지는 각종 임상과 관련된 검사가 기술적 요건과 신뢰성을 갖췄다는 것을 보장하는 국제표준이다.인증을 받음으로써 아프리글로벌 메디케어는 국내에서 대단히 필요하고 품질을 갖춘 진단 서비스를 제공하는 장기 전략 여행에 요구되는 필수적인 디딤돌을 마련한 것으로 평가받는다.나이지리아 승인 서비스의 의료연구소과학위원회(Medical Laboratory Science Council)가 표준 인증을 위한 감사 작업을 진행했다. 인증을 받은 핵심 노하우는 2가지로 요약된다.첫째, 베스트 프랙티스에 기반한 운영을 활용하는 글로벌 수준의 시스템을 갖춘 연구소를 건설했다. 둘째, 연구소는 고객과 사회를 위해 최고 수준의 품질 표준을 운영하기 위해 노력했다.참고로 아프리글로벌 메디케어는 매일 3500건 이상의 샘플을 분석해 질병을 진단한다. 코로나19 진단을 포함해 1일 24시간 365일 운영 중이다. -
![[네델란드] 유럽 의약품청(EMA), 세균 감염 치료를 위한 인체 의약품 평가에 대한 최종 지침 발표](http://www.stdnews.kr/data/file/news/thumb/thumb-988342002_WSN2r4lM_150bd32913d409f81b0c3321556bbb481552e81d_200x180.jpg) [네델란드] 유럽 의약품청(EMA), 세균 감염 치료를 위한 인체 의약품 평가에 대한 최종 지침 발표네델란드 암스테르담에 위치한 유럽 의약품청(European Medicines Agency, EMA)에 따르면 새로운 항생제 개발을 지원하기 위해 세균 감염 치료를 위한 인체 의약품 평가에 대한 최종 지침을 발표했다.인체 의약품 평가 최종 지침은 박테리아 감염 치료를 위한 새로운 향균제 개발에 대한 글로벌 접근법을 지원하기 위한 목적으로 제정됐다.개정된 지침은 2019년 발표돼 6개월간 공개 협의를 거쳤다. 최종 문서는 2022년 5월 EMA의 인체 의약품 위원회(CHMP)에서 채택했다.향균 치료에 저항하는 미생물의 능력인 항균제 내성(Antimicrobial resistance, AMR), 특히 항생제는 사람과 동물의 건강에 직접적으로 영향을 미친다.AMR로 인해 유럽연합(EU)에서만 매년 3만3000명이 사망하고 있다. 연간 15억 유로의 의료 비용과 생산성 손실을 발생하는 것으로 추정된다. 따라서 전 세계적으로 재정 손실을 야기시키고 있다.따라서 EMA는 인체 의약품 평가에 대한 최종 지침 발표뿐 아니라 신규 의약품 및 치료 접근법 개발을 지도하고 지원하기 위한 노력하고 있다.특히 현재 치료법이 거의 없는 다제내성 박테리아에 의한 감염을 가진 환자들을 위해 싸우고 있다. 세계적으로 향균제 내성은 대단히 위협적이다.EU와 미국, 일본의 규제 당국은 각각의 데이터 요건을 조정해 의약품 개발자가 여러 규제기관의 증거 요구를 충족하는 임상 시험을 설계할 수 있도록 했다.개정된 문서에는 충족되지 않은 요구를 해결하기 위한 향균제의 권장 임상 개발 프로그램에 대한 설명이 포함된다.합병증이 없는 요로 감염 및 임질 치료를 지원하기 위한 임상 시험에 대한 지침, 제품 특성 요약에 미생물학적 및 임상적 효능 데이터 표시에 대한 업데이트된 지침 등이 있다.또한 개정된 지침 부록에는 소아에서의 세균 감염에 관한 내용이 포함됐다. 소아 세균 감염 치료를 위한 의약품 허가 지원에 필요한 임상 개발 프로그램을 조정하려는 목적이다.일부 감염 치료를 위해 성인의 효능 데이터를 살펴서 특정 어린이 연령 그룹에 효능의 결과를 추정할 수 있다. 부록에 새로운 항생제 개발회사들이 외삽 개념을 개발하고 외삽 계획에 대해 자세한 내용을 제공하도록 하고 있다.특히 특정 연령 이하 어린이에게만 발생하거나 대부분 발생하는 일부 감염의 경우 성인의 효능 데이터로 추정하는 것은 불가능하다. 따라서 예외적인 경우에 시행할 수 있는 시험에 대한 지침이 포함돼 있다.참고로 외삽법이란 미래예측 기법으로 과거 데이터 결과가 미래에도 그대로 지속될 것이라는 가정하에 과거 추세선을 연장해 미래 시점을 예측하는 것을 말한다.
[네델란드] 유럽 의약품청(EMA), 세균 감염 치료를 위한 인체 의약품 평가에 대한 최종 지침 발표네델란드 암스테르담에 위치한 유럽 의약품청(European Medicines Agency, EMA)에 따르면 새로운 항생제 개발을 지원하기 위해 세균 감염 치료를 위한 인체 의약품 평가에 대한 최종 지침을 발표했다.인체 의약품 평가 최종 지침은 박테리아 감염 치료를 위한 새로운 향균제 개발에 대한 글로벌 접근법을 지원하기 위한 목적으로 제정됐다.개정된 지침은 2019년 발표돼 6개월간 공개 협의를 거쳤다. 최종 문서는 2022년 5월 EMA의 인체 의약품 위원회(CHMP)에서 채택했다.향균 치료에 저항하는 미생물의 능력인 항균제 내성(Antimicrobial resistance, AMR), 특히 항생제는 사람과 동물의 건강에 직접적으로 영향을 미친다.AMR로 인해 유럽연합(EU)에서만 매년 3만3000명이 사망하고 있다. 연간 15억 유로의 의료 비용과 생산성 손실을 발생하는 것으로 추정된다. 따라서 전 세계적으로 재정 손실을 야기시키고 있다.따라서 EMA는 인체 의약품 평가에 대한 최종 지침 발표뿐 아니라 신규 의약품 및 치료 접근법 개발을 지도하고 지원하기 위한 노력하고 있다.특히 현재 치료법이 거의 없는 다제내성 박테리아에 의한 감염을 가진 환자들을 위해 싸우고 있다. 세계적으로 향균제 내성은 대단히 위협적이다.EU와 미국, 일본의 규제 당국은 각각의 데이터 요건을 조정해 의약품 개발자가 여러 규제기관의 증거 요구를 충족하는 임상 시험을 설계할 수 있도록 했다.개정된 문서에는 충족되지 않은 요구를 해결하기 위한 향균제의 권장 임상 개발 프로그램에 대한 설명이 포함된다.합병증이 없는 요로 감염 및 임질 치료를 지원하기 위한 임상 시험에 대한 지침, 제품 특성 요약에 미생물학적 및 임상적 효능 데이터 표시에 대한 업데이트된 지침 등이 있다.또한 개정된 지침 부록에는 소아에서의 세균 감염에 관한 내용이 포함됐다. 소아 세균 감염 치료를 위한 의약품 허가 지원에 필요한 임상 개발 프로그램을 조정하려는 목적이다.일부 감염 치료를 위해 성인의 효능 데이터를 살펴서 특정 어린이 연령 그룹에 효능의 결과를 추정할 수 있다. 부록에 새로운 항생제 개발회사들이 외삽 개념을 개발하고 외삽 계획에 대해 자세한 내용을 제공하도록 하고 있다.특히 특정 연령 이하 어린이에게만 발생하거나 대부분 발생하는 일부 감염의 경우 성인의 효능 데이터로 추정하는 것은 불가능하다. 따라서 예외적인 경우에 시행할 수 있는 시험에 대한 지침이 포함돼 있다.참고로 외삽법이란 미래예측 기법으로 과거 데이터 결과가 미래에도 그대로 지속될 것이라는 가정하에 과거 추세선을 연장해 미래 시점을 예측하는 것을 말한다. -
![[미국] 사이버포트, ISO 27002:2022 표준의 재구성 공개](http://www.stdnews.kr/data/file/news/thumb/thumb-988342002_D4dMJvic_1b2263406acbf214f626f1af7b199f4eff0288cf_200x180.jpg) [미국] 사이버포트, ISO 27002:2022 표준의 재구성 공개미국 사이버 보안 서비스 제공업체인 사이버포트 그룹(Cyberfort Group)에 따르면 2022년 2월 ISO 27002:2022 표준이 새로 재구성되어 공개됐다.표준을 최신 상태로 유지하기 위한 목적이다. ISO 27001은 정보 보안을 관리하는 시스템에 대한 표준으로서 정보 보안 관리 시스템에 대한 요구사항을 정의해 조직이 정보 자산을 보호할 수 있도록 지원한다.ISO 27002는 ISO 27001에 나열된 제어를 구현하는 방법에 대한 표준이다. IS 27002는 2013년 114개의 제어 표준이 존재했지만 2022년 93개로 축소됐다.ISO 27002:2022의 새로운 표준은 코로나 전염벙(Pandemic)과 하이브리드 작업 모델(hybrid work model)의 영향을 받지는 않았다. 새로운 표준을 구현하는 데에 몇년이 걸리기 때문이다.ISO 27002:2022의 제어기능 중 하나가 필요성이 증가하고 있는 클라우드 서비스와 관련돼 있다. ISO 27002:2022의 기본 구성에 대한 요약은 아래와 같다.ISO/IEC 27002:2022는 구현 지침을 포함한 일반 정보 보안 제어의 참조 세트를 제공한다. 다음 조직에서 사용하도록 설계됐다.a) ISO/IEC27001에 기반한 정보보안관리시스템(ISMS)의 맥락 내b) 국제적으로 인정된 모범 사례를 기반으로 정보보안 통제 구현c) 조직별 정보보안 관리 지침 개발
[미국] 사이버포트, ISO 27002:2022 표준의 재구성 공개미국 사이버 보안 서비스 제공업체인 사이버포트 그룹(Cyberfort Group)에 따르면 2022년 2월 ISO 27002:2022 표준이 새로 재구성되어 공개됐다.표준을 최신 상태로 유지하기 위한 목적이다. ISO 27001은 정보 보안을 관리하는 시스템에 대한 표준으로서 정보 보안 관리 시스템에 대한 요구사항을 정의해 조직이 정보 자산을 보호할 수 있도록 지원한다.ISO 27002는 ISO 27001에 나열된 제어를 구현하는 방법에 대한 표준이다. IS 27002는 2013년 114개의 제어 표준이 존재했지만 2022년 93개로 축소됐다.ISO 27002:2022의 새로운 표준은 코로나 전염벙(Pandemic)과 하이브리드 작업 모델(hybrid work model)의 영향을 받지는 않았다. 새로운 표준을 구현하는 데에 몇년이 걸리기 때문이다.ISO 27002:2022의 제어기능 중 하나가 필요성이 증가하고 있는 클라우드 서비스와 관련돼 있다. ISO 27002:2022의 기본 구성에 대한 요약은 아래와 같다.ISO/IEC 27002:2022는 구현 지침을 포함한 일반 정보 보안 제어의 참조 세트를 제공한다. 다음 조직에서 사용하도록 설계됐다.a) ISO/IEC27001에 기반한 정보보안관리시스템(ISMS)의 맥락 내b) 국제적으로 인정된 모범 사례를 기반으로 정보보안 통제 구현c) 조직별 정보보안 관리 지침 개발 -
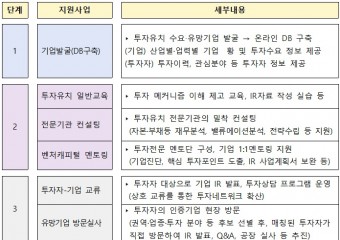
![[미국] 특허청, 심사 중 프리어필(Pre-Appeal) 제도의 활용](http://www.stdnews.kr/data/file/news/thumb/thumb-3698709524_5yg3zAcu_1f42e80ab3772061105a031768998abd15319cdf_200x180.jpg) [미국] 특허청, 심사 중 프리어필(Pre-Appeal) 제도의 활용미국 특허 출원의 경우에 심사 중 최종거절통지서(Final Office Action) 통지를 받으면 3개월 내에 답변서를 제출해야 한다. 총 6개월까지 연장이 가능하다. 이 때, 출원인은 미국 특허법이 허용하는 절차에 따라 다양한 대응 방법을 선택할 수 있다. 이 중에서 심사관의 결정에 대해 심판부(PTAB)에 불복심판(Appeal)을 진행하기에 앞서 심사관 3인의 합의체에 의해 비교적 간단히 심사를 받을 수 있는 프리어필(Pre-Appeal)제도가 이용될 수 있다. 불복심판(Appeal)의 경우에는 많은 비용과 시간이 소요된다는 단점이 있기 때문이다. 프리어필(Pre-Appeal) 제도를 요약하면 하기와 같다. 요약 : Pre-Appeal Brief Conference 1. 목적 : 비용 및 시간 부담을 줄이면서 Appeal 단계에서의 Appeal brief 제출 이전에 심사관 3인(심사관, 감독관, 다른 심사관)에 의해 재심사되는 프로그램 2. 요건 1) 5페이지의 의견서 제출 2) 심사관의 거절에 대한 심사관의 명백한 오류 3) 청구항 또는 선행기술에 대한 심사관의 해석에 대한 반박은 불가능 3. 결과 1) Appeal을 위한 실제적인 이슈가 있는 경우에는 appeal 절차를 계속 진행 2) 새로운 거절이 있거나 심사관의 보정이 있는 경우에는 기존 심사절차 재오픈(기존 심사관의 거절은 극복되었지만 새로운 조사 등의 필요) 3) 기존 청구항의 등록 허여 4. 효과 명백하게 부당한 거절이유를 다른 경험 있는 심사관들이 함께 검토해 부당한 거절이유를 철회하도록 함으로써 Appeal이나 RCE로 인행 발생되는 비용 및 시간 부담을 줄이도록 함. 5. 통계 1) Appeal 중 약 40% 건에 대해 Pre-Appeal 진행 2) Pre-Appeal 건 중 약 55%는 Appeal 계속 진행 3) Pre-Appeal 건 중 약 35%는 기존 심사절차 재오픈 4) Pre-Appeal 건 중 약 10%는 바로 등록 허여
[미국] 특허청, 심사 중 프리어필(Pre-Appeal) 제도의 활용미국 특허 출원의 경우에 심사 중 최종거절통지서(Final Office Action) 통지를 받으면 3개월 내에 답변서를 제출해야 한다. 총 6개월까지 연장이 가능하다. 이 때, 출원인은 미국 특허법이 허용하는 절차에 따라 다양한 대응 방법을 선택할 수 있다. 이 중에서 심사관의 결정에 대해 심판부(PTAB)에 불복심판(Appeal)을 진행하기에 앞서 심사관 3인의 합의체에 의해 비교적 간단히 심사를 받을 수 있는 프리어필(Pre-Appeal)제도가 이용될 수 있다. 불복심판(Appeal)의 경우에는 많은 비용과 시간이 소요된다는 단점이 있기 때문이다. 프리어필(Pre-Appeal) 제도를 요약하면 하기와 같다. 요약 : Pre-Appeal Brief Conference 1. 목적 : 비용 및 시간 부담을 줄이면서 Appeal 단계에서의 Appeal brief 제출 이전에 심사관 3인(심사관, 감독관, 다른 심사관)에 의해 재심사되는 프로그램 2. 요건 1) 5페이지의 의견서 제출 2) 심사관의 거절에 대한 심사관의 명백한 오류 3) 청구항 또는 선행기술에 대한 심사관의 해석에 대한 반박은 불가능 3. 결과 1) Appeal을 위한 실제적인 이슈가 있는 경우에는 appeal 절차를 계속 진행 2) 새로운 거절이 있거나 심사관의 보정이 있는 경우에는 기존 심사절차 재오픈(기존 심사관의 거절은 극복되었지만 새로운 조사 등의 필요) 3) 기존 청구항의 등록 허여 4. 효과 명백하게 부당한 거절이유를 다른 경험 있는 심사관들이 함께 검토해 부당한 거절이유를 철회하도록 함으로써 Appeal이나 RCE로 인행 발생되는 비용 및 시간 부담을 줄이도록 함. 5. 통계 1) Appeal 중 약 40% 건에 대해 Pre-Appeal 진행 2) Pre-Appeal 건 중 약 55%는 Appeal 계속 진행 3) Pre-Appeal 건 중 약 35%는 기존 심사절차 재오픈 4) Pre-Appeal 건 중 약 10%는 바로 등록 허여 -
![[미국] 특허청, 등록결정 후 등록료 납부 전에 QPIDS 이용 가능](http://www.stdnews.kr/data/file/news/thumb/thumb-3698709524_n5KZjPHr_f961913c233147876b9337aebc51e8700b773608_200x180.jpg) [미국] 특허청, 등록결정 후 등록료 납부 전에 QPIDS 이용 가능미국에서 특허를 출원할 경우에 등록결정 후 등록료 납부 전에 정보공개진술서(Information Disclosure Statement, IDS)를 제출해야 하는 경우가 발생될 수 있다. 이때 계속심사청구(Request for Continued Examination, RCE) 제출 후 prosecution reopening없이도 IDS를 처리할 수 있도록 QPIDS(Quick Path Information Disclosure Statement) 프로그램을 이용할 수 있다.특허 등록료 납부 후 미처 제출하지 못한 문헌이 존재한다는 이유만으로 불필요한 계속심사청구(RCE)가 신청되는 것을 방지하기 위한 목적이다. QPIDS를 요약하면 아래와 같다.요약 - QPIDS1. 정의 : 등록료(issue fee)를 납부한 이후에 IDS를 제출해야 할 필요가 생기는 경우, 계속심사청구(RCE) 제출에 이은 prosecution reopening없이도 IDS를 처리할 수 있도록 해주는 파일럿 프로그램.2. 요건 1) Issue fee payment이후 issuance 이전 2) QPIDS petition transmittal (PTO/SB/09) 제출 – 관납료 없음 3) IDS form and fee ($180) 4) Petition to withdraw from issue after issue fee payment (본 petition fee $140) 5) RCE request and fee (1차 RCE $1200, 2차 이후 $1700) – 조건부 RCE로 일단 제출함.3. 이후 절차 (심사관) 1) 제출된 IDS가 특허성에 영향이 없을 경우에 심사관은 corrected NOA를 발행(IDS considered)하고, issue로 계속 진행함(RCE fee는 refund 됨) 2) 제출된 IDS가 특허성에 영향이 있을 경우(if the IDS necessitates reopening prosecution), 새로운 OA를 발행(RCE fee는 refund되지 않음). 3) 최종적으로 해당 출원이 NOA를 받을 경우, 이전에 납부한 issue fee가 reapply될 수 있으므로, 그러한 request를 하면 issue fee를 다시 낼 필요는 없음.4) 효과기존에는 예외없이 RCE제출에 이어 prosecution reopen을 해야함에 따라 출원인이 시간 및 비용상 상당한 손해를 감수해야만 했다. 하지만 본 program을 이용해 prosecution reopen의 필요가 없다고 판단될 경우, 출원인이 시간상 (prosecution reopen없이 issue로 계속 진행) 및 비용상 (RCE fee 환불) 손해를 감수하지 않아도 됨.
[미국] 특허청, 등록결정 후 등록료 납부 전에 QPIDS 이용 가능미국에서 특허를 출원할 경우에 등록결정 후 등록료 납부 전에 정보공개진술서(Information Disclosure Statement, IDS)를 제출해야 하는 경우가 발생될 수 있다. 이때 계속심사청구(Request for Continued Examination, RCE) 제출 후 prosecution reopening없이도 IDS를 처리할 수 있도록 QPIDS(Quick Path Information Disclosure Statement) 프로그램을 이용할 수 있다.특허 등록료 납부 후 미처 제출하지 못한 문헌이 존재한다는 이유만으로 불필요한 계속심사청구(RCE)가 신청되는 것을 방지하기 위한 목적이다. QPIDS를 요약하면 아래와 같다.요약 - QPIDS1. 정의 : 등록료(issue fee)를 납부한 이후에 IDS를 제출해야 할 필요가 생기는 경우, 계속심사청구(RCE) 제출에 이은 prosecution reopening없이도 IDS를 처리할 수 있도록 해주는 파일럿 프로그램.2. 요건 1) Issue fee payment이후 issuance 이전 2) QPIDS petition transmittal (PTO/SB/09) 제출 – 관납료 없음 3) IDS form and fee ($180) 4) Petition to withdraw from issue after issue fee payment (본 petition fee $140) 5) RCE request and fee (1차 RCE $1200, 2차 이후 $1700) – 조건부 RCE로 일단 제출함.3. 이후 절차 (심사관) 1) 제출된 IDS가 특허성에 영향이 없을 경우에 심사관은 corrected NOA를 발행(IDS considered)하고, issue로 계속 진행함(RCE fee는 refund 됨) 2) 제출된 IDS가 특허성에 영향이 있을 경우(if the IDS necessitates reopening prosecution), 새로운 OA를 발행(RCE fee는 refund되지 않음). 3) 최종적으로 해당 출원이 NOA를 받을 경우, 이전에 납부한 issue fee가 reapply될 수 있으므로, 그러한 request를 하면 issue fee를 다시 낼 필요는 없음.4) 효과기존에는 예외없이 RCE제출에 이어 prosecution reopen을 해야함에 따라 출원인이 시간 및 비용상 상당한 손해를 감수해야만 했다. 하지만 본 program을 이용해 prosecution reopen의 필요가 없다고 판단될 경우, 출원인이 시간상 (prosecution reopen없이 issue로 계속 진행) 및 비용상 (RCE fee 환불) 손해를 감수하지 않아도 됨. -
![[영국] 유럽 의약품청(EMA), EMRN이 EU의 전자제품 정보(ePI)에 관한 공통 표준 채택](http://www.stdnews.kr/data/file/news/thumb/thumb-3698709524_FHK2U3wi_701607cec589e9e068ea38ce760d6a73bba14a54_200x180.jpg) [영국] 유럽 의약품청(EMA), EMRN이 EU의 전자제품 정보(ePI)에 관한 공통 표준 채택유럽 의약품청(European Medicines Agency, EMA)에 따르면 유럽 의약규제 네트워크(European Medicines Regulatory Network, EMRN)가 유럽연합(European Union, EU)의 전자제품 정보(electronic product information, ePI)에 관한 공통 표준을 채택했다.이번 표준 채택으로 EU의 환자들이 확장된 전자채널을 통해 모든 의약품의 최신 정보를 이용할 수 있게 됐다. 의약 제품 정보에는 환자를 위한 패키지 전단 및 의료 전문가를 위한 제품 특성 요약(summary of product characteristics, SmPC)등이 포함된다.EU ePI 공통 표준은 유럽 내 의약품에 관한 조화된 전자 정보의 제공을 지원한다. 환자, 소비자, 의료 전문가를 위한 정보 제공을 개선하기 위해 마련됐다.ePI의 구조화된 특성은 제품 정보를 개별 요구에 맞게 개인화해 새로운 기회를 제공한다. 또한 다양한 능력을 가진 사용자가 쉽게 접근할 수 있도록 한다.채택된 ePI는 새로운 정보가 나오면 즉시 수정될 수 있다. 향후 개발은 자동 업데이트 알림, 지원 비디오 또는 오디오 콘텐츠에 대한 접근, 온라인 부작용 보고 도구 와 같은 기능이 포함될 수 있다.공통 표준은 2021년 EMA, NCA(national competent authorities), EC(European Commission)에서 수행한 ePI 프로젝트의 주요 결과물 중 하나이다.EU의 자금 지원 프로그램인 EU4Health에 의해 지원되는 후속 파일럿 프로젝트는 현재 구현에 앞서 ePI 사용을 테스트하기 위한 도구 및 지침 개발에 초점을 맞추고 있다.EMA에 따르면 정기적인 진행 상황 업데이트를 게시하고 그 결과를 환자, 의료 전문가, 학계 및 제약 업계와 공유할 예정이다.EU의 ePI 공통 표준은 데이터 포맷 및 요소, 전자 건강 기록 교환을 위한 어플리케이션 프로그램 인터페이스를 설명하는 국제기술표준 FHIR(Fast Healthcare Interoperability Resources)를 기반으로 하고 있다.참고로 FHIR은 유럽 의약품 규제 네트워크에 의약품, 물질 및 관련 참조 데이터에 관한 정보 교환을 지원하고 있다.
[영국] 유럽 의약품청(EMA), EMRN이 EU의 전자제품 정보(ePI)에 관한 공통 표준 채택유럽 의약품청(European Medicines Agency, EMA)에 따르면 유럽 의약규제 네트워크(European Medicines Regulatory Network, EMRN)가 유럽연합(European Union, EU)의 전자제품 정보(electronic product information, ePI)에 관한 공통 표준을 채택했다.이번 표준 채택으로 EU의 환자들이 확장된 전자채널을 통해 모든 의약품의 최신 정보를 이용할 수 있게 됐다. 의약 제품 정보에는 환자를 위한 패키지 전단 및 의료 전문가를 위한 제품 특성 요약(summary of product characteristics, SmPC)등이 포함된다.EU ePI 공통 표준은 유럽 내 의약품에 관한 조화된 전자 정보의 제공을 지원한다. 환자, 소비자, 의료 전문가를 위한 정보 제공을 개선하기 위해 마련됐다.ePI의 구조화된 특성은 제품 정보를 개별 요구에 맞게 개인화해 새로운 기회를 제공한다. 또한 다양한 능력을 가진 사용자가 쉽게 접근할 수 있도록 한다.채택된 ePI는 새로운 정보가 나오면 즉시 수정될 수 있다. 향후 개발은 자동 업데이트 알림, 지원 비디오 또는 오디오 콘텐츠에 대한 접근, 온라인 부작용 보고 도구 와 같은 기능이 포함될 수 있다.공통 표준은 2021년 EMA, NCA(national competent authorities), EC(European Commission)에서 수행한 ePI 프로젝트의 주요 결과물 중 하나이다.EU의 자금 지원 프로그램인 EU4Health에 의해 지원되는 후속 파일럿 프로젝트는 현재 구현에 앞서 ePI 사용을 테스트하기 위한 도구 및 지침 개발에 초점을 맞추고 있다.EMA에 따르면 정기적인 진행 상황 업데이트를 게시하고 그 결과를 환자, 의료 전문가, 학계 및 제약 업계와 공유할 예정이다.EU의 ePI 공통 표준은 데이터 포맷 및 요소, 전자 건강 기록 교환을 위한 어플리케이션 프로그램 인터페이스를 설명하는 국제기술표준 FHIR(Fast Healthcare Interoperability Resources)를 기반으로 하고 있다.참고로 FHIR은 유럽 의약품 규제 네트워크에 의약품, 물질 및 관련 참조 데이터에 관한 정보 교환을 지원하고 있다. -
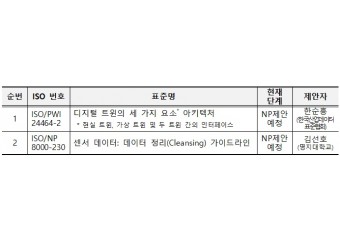
![[미국] 미국 특허 정보공개진술서(IDS) 제출 의무](http://www.stdnews.kr/data/file/news/thumb/thumb-3698709524_quFafA2y_0ab8256d3a2e221db3de34db917ea971de99ca6d_200x180.jpg) [미국] 미국 특허 정보공개진술서(IDS) 제출 의무미국은 특허를 출원할 때에 정보공개진술서(IDS: Information Disclosure Statement)를 제출해야 하는 공개 의무(duty of disclosure)가 출원인과 대리인에게 주어진다(미 연방규칙 37 C.F.R. §1.56(a)).해당 의무를 지키지 않았을 경우에는 불공정한 행위로 인정될 수 있으며 소송 시 특허의 권리행사가 불가능하게 될 수 있다. 치열한 글로벌 특허 전쟁에서 이와 같은 IDS 제출 의무 위반은 손쉬운 공격 대상이 될 수 있다.IDS 제출 의무와 관련된 판례는 많지만 'Semiconductor Energy Laboratory Co. v. Samsung Electronics Co.' 2000년도 연방 항소법원 판례는 대표적인 경우이다.특히 개인이나 중소기업들은 이에 대한 이해가 부족한 경우가 많아 더욱 더 주의가 필요하다. 이와 같은 내용을 간략하게 요약하면 다음과 같다.요약1. 정의 : 출원인이 발명한 내용과 가장 유사한 문헌들에 대해 자진해 미국 특허청에 제출해야 하는 의무2. 개시 의무자 : 발명자, 권리의 양수인(출원인), 변호사, 발명자/출원인의 법률 보조인3. 제출 대상 문헌 : 특허, 특허출원, 반포된 문헌, 실험적 이용 및 테스트 자료4. 제출 시기 : 미 연방규칙 37 C.F.R. §1.97에 정해진 절차와 요건에 따라 제출 1) 1단계 : 실체적 내용에 대한 최초의 거절이유(first office action) 통지를 받기 전 또는 미국 출원일로부터 3개월 내에 제출 – 비용이나 증명서 불필요 2) 2 단계 : 1단계 이후 최종거절이유(final office action) 통지, 등록통지(notice of allowance) 중 하나라도 발생되기 이전 - 37 C.F.R. §1.97(e)에 규정된 진술서 함께 제출(최초로 인지한 때부터 3개월 이내) 또는 37 C.F.R. §1.17(p)에 규정된 수수료 납부(최초로 인지한 때부터 3개월 경과한 경우) 3) 3 단계 : 최종거절이유 통지, 등록통지 중 하나라도 발생한 이후부터 등록료 납부 이전 - 37 C.F.R. §1.97(e)에 규정된 진술서 및 37 C.F.R. §1.17(p)에 규정된 수수료 함께 납부 4) 4 단계 : 등록료 납부 후 등록공보 발행(issue) 전 – Petition 함께 제출5. 미제출 시 : 권리행사 제한
[미국] 미국 특허 정보공개진술서(IDS) 제출 의무미국은 특허를 출원할 때에 정보공개진술서(IDS: Information Disclosure Statement)를 제출해야 하는 공개 의무(duty of disclosure)가 출원인과 대리인에게 주어진다(미 연방규칙 37 C.F.R. §1.56(a)).해당 의무를 지키지 않았을 경우에는 불공정한 행위로 인정될 수 있으며 소송 시 특허의 권리행사가 불가능하게 될 수 있다. 치열한 글로벌 특허 전쟁에서 이와 같은 IDS 제출 의무 위반은 손쉬운 공격 대상이 될 수 있다.IDS 제출 의무와 관련된 판례는 많지만 'Semiconductor Energy Laboratory Co. v. Samsung Electronics Co.' 2000년도 연방 항소법원 판례는 대표적인 경우이다.특히 개인이나 중소기업들은 이에 대한 이해가 부족한 경우가 많아 더욱 더 주의가 필요하다. 이와 같은 내용을 간략하게 요약하면 다음과 같다.요약1. 정의 : 출원인이 발명한 내용과 가장 유사한 문헌들에 대해 자진해 미국 특허청에 제출해야 하는 의무2. 개시 의무자 : 발명자, 권리의 양수인(출원인), 변호사, 발명자/출원인의 법률 보조인3. 제출 대상 문헌 : 특허, 특허출원, 반포된 문헌, 실험적 이용 및 테스트 자료4. 제출 시기 : 미 연방규칙 37 C.F.R. §1.97에 정해진 절차와 요건에 따라 제출 1) 1단계 : 실체적 내용에 대한 최초의 거절이유(first office action) 통지를 받기 전 또는 미국 출원일로부터 3개월 내에 제출 – 비용이나 증명서 불필요 2) 2 단계 : 1단계 이후 최종거절이유(final office action) 통지, 등록통지(notice of allowance) 중 하나라도 발생되기 이전 - 37 C.F.R. §1.97(e)에 규정된 진술서 함께 제출(최초로 인지한 때부터 3개월 이내) 또는 37 C.F.R. §1.17(p)에 규정된 수수료 납부(최초로 인지한 때부터 3개월 경과한 경우) 3) 3 단계 : 최종거절이유 통지, 등록통지 중 하나라도 발생한 이후부터 등록료 납부 이전 - 37 C.F.R. §1.97(e)에 규정된 진술서 및 37 C.F.R. §1.17(p)에 규정된 수수료 함께 납부 4) 4 단계 : 등록료 납부 후 등록공보 발행(issue) 전 – Petition 함께 제출5. 미제출 시 : 권리행사 제한 -
![[미국] 특허청, 최후 거절 후 대응 프로그램 AFCP 2.0 활용 가능](http://www.stdnews.kr/data/file/news/thumb/thumb-3698709524_IFNn8L2h_6d865212c8b7765f81e3d2208258949c46893ef5_200x180.jpg) [미국] 특허청, 최후 거절 후 대응 프로그램 AFCP 2.0 활용 가능미국 특허청(USPTO)은 최종 거절이유 통지(Final Office Action)가 발행된 이후 이에 대한 대응을 간소화하기 위해 AFCP((After Final Consideration Pilot) 2.0 프로그램을 운영하고 있다.이 프로그램은 최종 결정을 재고려할 수 있도록 추가적인 시간을 허용하는 미국 특허청의 최후 거절 후의 보정범위 완화 프로그램이다.AFCP 2.0은 최종 거절 이유 통지 이후 출원인이 다양하게 대응할 수 있도록 출원인의 선택 범위를 확장해 줄 수 있다.특히 출원인의 대응 전략이 실패하더라도 심사관으로부터 Adivisory Action이 발행되면 계속심사청구(Request for Continued Examination) 또는 심판(Appeal) 청구 등의 다음과 같은 대응전략을 결정할 수 있다.요약 1. 정의 : 최종거절통지의 답변(after-final response)에서 독립항의 범위를 넓히지 않는 보정을 행하면, 추가적인 관납료(fee)없이 심사관이 그 보정을 고려할 수 있도록 하는 파일럿 프로그램(pilot program).2. 목적 : 비용 및 시간 부담을 줄이면서 특허청에 계류정인 재심사(RCE) 건의 숫자를 줄이기 위한 심사관과 출원인의 협력3. 요건 : 1)가출원, 계속출원, 분할출원 대상(reissue 또는 Reexamination 불가능) 2)최소 1개 이상의 독립항의 수정(청구항의 확장은 불가능) 3)심사관과의 인터뷰에 참여한다는 진술서(statement) 제출 4)e-filing으로 진행해야 함(EFS-Web)4. 이후 절차(심사관) 1)요건에 따라 제출되면 심사관은 3시간 이내에 재고려 가능한지 아니면 추가의 조사가 필요한지를 판단 2)재고려 가능한 경우에는 보정안의 등록여부를 판단 3)등록이 어려운 경우에는 대리인과 인터뷰 진행(선택사항) 4)등록이 가능한 경우에는 Notice Of Allowance 발행 5)상기 절차에서 추가의 조사가 필요한 경우이거나, 대리인과 인터뷰 결과에 대해 Advisory Action을 발행
[미국] 특허청, 최후 거절 후 대응 프로그램 AFCP 2.0 활용 가능미국 특허청(USPTO)은 최종 거절이유 통지(Final Office Action)가 발행된 이후 이에 대한 대응을 간소화하기 위해 AFCP((After Final Consideration Pilot) 2.0 프로그램을 운영하고 있다.이 프로그램은 최종 결정을 재고려할 수 있도록 추가적인 시간을 허용하는 미국 특허청의 최후 거절 후의 보정범위 완화 프로그램이다.AFCP 2.0은 최종 거절 이유 통지 이후 출원인이 다양하게 대응할 수 있도록 출원인의 선택 범위를 확장해 줄 수 있다.특히 출원인의 대응 전략이 실패하더라도 심사관으로부터 Adivisory Action이 발행되면 계속심사청구(Request for Continued Examination) 또는 심판(Appeal) 청구 등의 다음과 같은 대응전략을 결정할 수 있다.요약 1. 정의 : 최종거절통지의 답변(after-final response)에서 독립항의 범위를 넓히지 않는 보정을 행하면, 추가적인 관납료(fee)없이 심사관이 그 보정을 고려할 수 있도록 하는 파일럿 프로그램(pilot program).2. 목적 : 비용 및 시간 부담을 줄이면서 특허청에 계류정인 재심사(RCE) 건의 숫자를 줄이기 위한 심사관과 출원인의 협력3. 요건 : 1)가출원, 계속출원, 분할출원 대상(reissue 또는 Reexamination 불가능) 2)최소 1개 이상의 독립항의 수정(청구항의 확장은 불가능) 3)심사관과의 인터뷰에 참여한다는 진술서(statement) 제출 4)e-filing으로 진행해야 함(EFS-Web)4. 이후 절차(심사관) 1)요건에 따라 제출되면 심사관은 3시간 이내에 재고려 가능한지 아니면 추가의 조사가 필요한지를 판단 2)재고려 가능한 경우에는 보정안의 등록여부를 판단 3)등록이 어려운 경우에는 대리인과 인터뷰 진행(선택사항) 4)등록이 가능한 경우에는 Notice Of Allowance 발행 5)상기 절차에서 추가의 조사가 필요한 경우이거나, 대리인과 인터뷰 결과에 대해 Advisory Action을 발행 -
![[미국] 특허법, 명세서의 내용으로부터 청구범위의 내용 제한 시 “a clear and unmistakable disclaimer” 원칙 준수](http://www.stdnews.kr/data/file/news/thumb/thumb-3698709524_seG1AuyR_17f9dead6e291a07234060175139d4d5d0d6f371_200x180.jpg) [미국] 특허법, 명세서의 내용으로부터 청구범위의 내용 제한 시 “a clear and unmistakable disclaimer” 원칙 준수미국 특허법에 따르면 명세서의 내용으로부터 청구 범위의 내용을 제한할 경우에 “a clear and unmistakable disclaimer” 원칙을 준수해야 한다.특허권의 권리는 발명을 서술한 명세서에 작성된 청구항을 통해 확보할 수 있다. 이에 따라 서술된 청구항의 해석에 따라 권리범위가 적용될 수 있는 범위가 달라질 수 있으므로 이에 대한 이해는 매우 중요하다. 예를 들면 특허 명세서에 개시된 발명의 서면 설명에 비춰 특허의 청구를 해석해야 하는지 여부 또는 미국 항소 법원이 우선 청구조건의 일반적인 의미를 결정해야 하는지 여부도 하나의 중요한 요소가 될 수 있다.이에 대한 실례로서 컨티넨털 서킷(Continental Circuits)과 인텔(Intel)간의 소송을 소개한다. 이 판례에서는 특허권자가 주장 범위를 명확하고 명백하게 반박하지 않았다.그 과정이 청구된 발명의 필수 부분이라는 것을 명확하게 하지 않은 경우, 제품 청구를 제한적으로 해석하는 것은 부적절하다는 점을 보여준다.국문요약 : 본 판례는 청구항에 언급된 “surface”, “removal”, “etching”, “dielectric material’의 용어가 명세서에 언급된 “repeated desmear process”용어에 의해 한정되는지 여부에 관한 것이다.연방순회 항소법원에서는 비록 명세서에 “repeated desmear process” 용어가 사용됐지만 청구항에서는 이에 대한 용어가 직접 사용되지 않고 있다는 점을 언급하면서 지방법원의 잘못을 지적했다.또한 명세서의 내용으로부터 청구 범위의 내용을 제한할 때에는 반드시 “a clear and unmistakable disclaimer” 원칙을 준수해야 한다는 점을 언급했다.영문요약 : Incorporating Limitation from Specification(Issue of Claim Construction)Continental Circuits v. Intel (F.C. 2019)History: • Continental asserted four patents directed to a “multilayer electrical device … having a tooth structure” against Intel.• Claims included the limitations regarding “surface,” “removal,” “etching,” and “dielectric material.”• Issue: whether the claim construction of these terms should be limited to a repeated desmear process.District Court:• Interpreted the limitations to require repeated process.• Determined that the Continental characterized “The present invention” as using a repeated desmear process.• Specification also seems to distinguish the invention from the single desmear process in the prior art.Federal Circuit:• Held that district court erred in costruing the terms to require that the dielectric material be “produced by a repeated desmear process.”• The plain claim language does not include this repeated process and the specification does not unmistakably limit the claims to require this process.• Although the claims do not stand alone and must be read in view of the specification, FC held that none of the asserted claims actually recite a “repeated desmear process.”• Specification may include an intentional disclaimer, or disavowal, of claim scope, but it is not the case here.• FC acknowledged difficulty in determining between whether to construe the claims in light of the specification or improperly importing a limitation from the specification into the claims.• Must follow “a clear and unmistakable disclaimer” standard when importing limitations from specification to the claims.
[미국] 특허법, 명세서의 내용으로부터 청구범위의 내용 제한 시 “a clear and unmistakable disclaimer” 원칙 준수미국 특허법에 따르면 명세서의 내용으로부터 청구 범위의 내용을 제한할 경우에 “a clear and unmistakable disclaimer” 원칙을 준수해야 한다.특허권의 권리는 발명을 서술한 명세서에 작성된 청구항을 통해 확보할 수 있다. 이에 따라 서술된 청구항의 해석에 따라 권리범위가 적용될 수 있는 범위가 달라질 수 있으므로 이에 대한 이해는 매우 중요하다. 예를 들면 특허 명세서에 개시된 발명의 서면 설명에 비춰 특허의 청구를 해석해야 하는지 여부 또는 미국 항소 법원이 우선 청구조건의 일반적인 의미를 결정해야 하는지 여부도 하나의 중요한 요소가 될 수 있다.이에 대한 실례로서 컨티넨털 서킷(Continental Circuits)과 인텔(Intel)간의 소송을 소개한다. 이 판례에서는 특허권자가 주장 범위를 명확하고 명백하게 반박하지 않았다.그 과정이 청구된 발명의 필수 부분이라는 것을 명확하게 하지 않은 경우, 제품 청구를 제한적으로 해석하는 것은 부적절하다는 점을 보여준다.국문요약 : 본 판례는 청구항에 언급된 “surface”, “removal”, “etching”, “dielectric material’의 용어가 명세서에 언급된 “repeated desmear process”용어에 의해 한정되는지 여부에 관한 것이다.연방순회 항소법원에서는 비록 명세서에 “repeated desmear process” 용어가 사용됐지만 청구항에서는 이에 대한 용어가 직접 사용되지 않고 있다는 점을 언급하면서 지방법원의 잘못을 지적했다.또한 명세서의 내용으로부터 청구 범위의 내용을 제한할 때에는 반드시 “a clear and unmistakable disclaimer” 원칙을 준수해야 한다는 점을 언급했다.영문요약 : Incorporating Limitation from Specification(Issue of Claim Construction)Continental Circuits v. Intel (F.C. 2019)History: • Continental asserted four patents directed to a “multilayer electrical device … having a tooth structure” against Intel.• Claims included the limitations regarding “surface,” “removal,” “etching,” and “dielectric material.”• Issue: whether the claim construction of these terms should be limited to a repeated desmear process.District Court:• Interpreted the limitations to require repeated process.• Determined that the Continental characterized “The present invention” as using a repeated desmear process.• Specification also seems to distinguish the invention from the single desmear process in the prior art.Federal Circuit:• Held that district court erred in costruing the terms to require that the dielectric material be “produced by a repeated desmear process.”• The plain claim language does not include this repeated process and the specification does not unmistakably limit the claims to require this process.• Although the claims do not stand alone and must be read in view of the specification, FC held that none of the asserted claims actually recite a “repeated desmear process.”• Specification may include an intentional disclaimer, or disavowal, of claim scope, but it is not the case here.• FC acknowledged difficulty in determining between whether to construe the claims in light of the specification or improperly importing a limitation from the specification into the claims.• Must follow “a clear and unmistakable disclaimer” standard when importing limitations from specification to the claims.


![[특집-ISO/IEC JTC 1/SC 17 활동] 35. Result of voting on SR Ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-3555379571_4cufp2BH_756bcefa64e6169e58646ad7b061ecbec455fb11_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 34. Result of voting on SR ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-3555380113_kIQxAlfN_727cc6e35ccb9d5e6c07574a3b3a2ab9db104d48_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 33. Result of voting on SR ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_R52GPIij_2bca2660198a937d2534db7bfd9fc8174a76cfa2_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 32. Result of voting on SR Ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_TxRrtYEa_c36d1a53acc15db7e18fae132ffef64e11bda43c_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 31. Result of voting on SR Ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-3555377690_nrjmWhSf_d9b63299e7f3f52053141cae28f32f7df40b5918_340x240.jpg)


![[일본] 요코하마(横浜), 3월 원격근무로 일하는 50대 여성이 장시간 노동을 강요받아 적응장애가 발병해 산재로 인정받아](http://www.stdnews.kr/data/file/news/thumb/thumb-3555377672_BapV2SmF_41a011a26290be1daa3f6a5220df7b8b6d167f69_340x240.jpg)
![[인도] 마하라슈트라주 식품의약국(Maharashtra FDA), 맥도날드 상품명에 치즈를 잘못 표기해 소비자 기만 지적](http://www.stdnews.kr/data/file/news/thumb/thumb-3743818281_Uu5GpcKZ_6890f33f4b087f58686ed20e46a04bbb79ad883e_340x240.jpg)
![[남아공] 토코만 푸드(Thokoman Foods), 자사 땅콩버터 식품 안전성 재확인](http://www.stdnews.kr/data/file/news/thumb/thumb-3743818281_h5HrK0kT_c2453abdb4577a16b34590f5b8f76de9c2a95469_340x240.jpg)
![[일본] 혼다(ホンダ), 2030년까지 전기자동차(EV)를 중심으로 하는 전동화와 소트프웨어 개발에 10조 엔을 투자할 계획](http://www.stdnews.kr/data/file/news/thumb/thumb-3555381172_1g5z7YDN_4db7699b271b5e9dbbe1a4f6dc69fb01a9881abb_340x240.jpg)
![[일본] 자민당(自民党), 기업이 직원을 고객의 '카스하라(カスハラ)로부터 보호를 의무로 하는 방안을 고려 중](http://www.stdnews.kr/data/file/news/thumb/thumb-3555381172_PCNyaL1v_9f9b79d526b4be07024401e874fe26f618a42e7c_340x240.jpg)
![[일본] 총무성(総務省), 2023년 기준 전국의 빈집은 900만 호로 사상 최고치 기록](http://www.stdnews.kr/data/file/news/thumb/thumb-3555379571_qr01mWC9_fef7fa874e596585a04ee2dae235376595341779_340x240.jpg)
![[특집-기상기후재난] 한국중부발전(주) 신정철 선임 인터뷰 - 행정안전부 뿐 아니라 기상기후 연계조직 모두가 참여하는 협의체가](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374516_iKWwUBas_9c1729f1e3977ee50c398986e7f98d5002a57deb_340x240.jpg)
![[특집-기상기후재난] (주)비밍코어 정성민 대표 인터뷰 - 인공지능(AI) 활용한 기후재난 대처 솔루션 개발](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374391_0JZYhIcj_dca23c54fc7923952082a9d7af92db00b9dd33c9_340x240.jpg)
![[기획-표준 전문가] 한국투자증권 김범수 FC 인터뷰 - 표준전문가 양성 교육이 지속되길 희망](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374114_Np9hM7aC_e6ffa916aade15e1c301badf3132ed3f0551a900_340x240.jpg)
![[특집-기상기후재난] 행정안전부 안전교육 전문인력 유정희 강사 인터뷰 - 기상기후재난예방 전문가 양성 시급](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374240_gOmdLG10_cfc17ed887dccc93f503013bf794ed568a5d40dc_340x240.jpg)
![[특집-기상기후재난] (주)이토스 김형식 대표 인터뷰 - 재난을 사전에 예측·예방할 기술개발 시급](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_lmUrCBIn_797dc8926bb7d90542546463cc73e6233f0bbb46_340x240.png)