검색결과
-
![[특집-기술위원회] TC 215 - 의료 정보학(Health informatics)](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_7HDAVCBF_87cd4effcac1b626d770aadf6bb9d9045d64b00f_200x180.jpg) [특집-기술위원회] TC 215 - 의료 정보학(Health informatics)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~107 △1963년 TC 108~111 △1964년 TC 112~115, TC 117 △1965년 TC 118 △1966년 TC 119~122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146~150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~161 △1975년 TC 162~164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171~174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~186 △1984년 TC 188 △1985년 TC 189~191 △1988년 TC 192~194 △1989년 TC 195 △1990년 TC 197, TC 198 △1991년 TC 199, TC 201, TC 202 △1992년 TC 204~206 △1993년 TC 209 △1994년 TC 210, TC 211 △1996년 TC 213, TC 214 등이 있다.ISO/TC 215 의료 정보학(Health informatics)과 관련된 기술위원회는 1998년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는 레이첼 호손(Ms Rachel Hawthorne)가 책임지고 있다. 현재 의장은 토드 쿠퍼(Mr Todd Cooper)이며 임기는 2026년 말까지다. ISO 기술 프로그램 관리자는 마호 다카하시(Mme Maho Takahashi), ISO 편집 관리자는 발레리아 아가넨노네(Ms Valeria Agamennone) 등이다.범위는 의료 관련 데이터, 의료 시스템의 모든 측면을 지원하고 활성화하는 지식의 수집, 교환 및 사용을 촉진하기 위한 의료 정보학 분야의 표준화다.현재 ISO/TC 215 사무국과 관련해 발행된 표준은 237개며 ISO/TC 215 사무국의 직접적인 책임 하에 발행된 표준은 225개다.ISO/TC 215과 관련해 개발 중인 표준은 64개며 이중 ISO/TC 215 사무국의 직접적인 책임 하에 개발 중인 표준은 62개다. 참여하고 있는 회원은 35개국, 참관 회원은 32개국이다.□ ISO/TC 215 사무국의 직접적인 책임 하에 발행된 표준 225개 중 15개 목록▷ISO 1828:2012 Health informatics — Categorial structure for terminological systems of surgical procedures▷ISO/TR 4421:2023 Health informatics — Introduction to Ayurveda informatics▷ISO/TS 5044:2023 Health informatics — Information model for quality control of traditional Chinese medicinal products▷ISO/TS 5118:2022 Health informatics — Categorial structure of representation for evaluation of clinical practice guidelines of traditional Chinese medicine▷ISO/TS 5346:2022 Health informatics — Categorial structure for representation of traditional Chinese medicine clinical decision support system▷ISO 5477:2023 Health informatics — Interoperability of public health emergency preparedness and response information systems▷ISO/TS 5499:2024 Health informatics — Clinical particulars — Core principles for the harmonization of therapeutic indications terms and identifiers▷ISO/TS 5568:2022 Health informatics — Traditional Chinese medicine — Labelling metadata of human biological sample information▷ISO/TS 5569:2023 Health informatics — Conceptual data model for Chinese medicinal herbs▷ISO/TR 9143:2023 Health informatics — Sex and gender in electronic health records▷ISO 10159:2011 Health informatics — Messages and communication — Web access reference manifest▷ISO 10781:2023 Health informatics — HL7 Electronic Health Record-System Functional Model, Release 2.1 (EHR FM)▷ISO/IEEE 11073-00103:2015 Health informatics — Personal health device communication — Part 00103: Overview▷ISO/IEEE 11073-10101:2020 Health informatics — Device interoperability — Part 10101: Point-of-care medical device communication — Nomenclature▷ISO/IEEE 11073-10102:2014 Health informatics — Point-of-care medical device communication — Part 10102: Nomenclature — Annotated ECG□ ISO/TC 215 사무국의 직접적인 책임 하에 개발 중인 표준 62개 중 15개 목록▷ISO/AWI TR 4419 Health informatics — Reducing clinicians burden▷ISO/DTS 5384 Health informatics - Categorial Structure and Data Elements for the Identification and Exchange of Immunization Data▷ISO/CD TS 5615 Health informatics — Accelerating Safe, Effective and Secure Remote Connected Care and Mobile Health Through Standards-Based Interoperability Solutions Addressing Gaps Revealed by Pandemics▷ISO/DTS 5777 Health informatics — The architecture of internet healthcare service network▷ISO/DTS 5788 Health informatics — Internet healthcare service pattern▷ISO/CD TS 6201.2 Health Informatics — Personalized Digital Health -Framework▷ISO/CD TS 6204 Health Informatics — Categorial structures for representation of Ayurvedic medicinal water — Decocting process in Ayurveda▷ISO/AWI TS 6226 Health informatics — Reference architecture for syndromic surveillance systems for infectious diseases▷ISO/DTR 6231 Health informatics — Standardizing graphical content▷ISO/CD TS 6268-1 Health informatics — Cybersecurity framework for telehealth environments — Part 1: Overview and Concepts▷ISO/AWI TS 6268-2 Health informatics — Cybersecurity framework for telehealth environments — Part 2: Cybersecurity reference models of telehealth▷ISO/CD TS 7122 Health Informatics — Guidelines for exchanging data generated by POCT (Point of Care Testing) devices between screening center and clinical laboratory▷ISO/AWI TS 9166 Health Informatics — Guidelines for self-assessment questionnaire systems▷ISO/DTS 9320 Health informatics — Standardized data set for transfer of hemodialysis patients▷ISO/DTS 9321 Health informatics — General requirements of multi-centre medical data collaborative analysis□ ISO/TC 215 사무국 분과위원회(Subcommittee)의 책임 하에 발행 및 개발 중인 표준 현황▷ISO/TC 215/SC 1 Genomics Informatics ; 발행된 표준 12개, 개발 중인 표준 2개
[특집-기술위원회] TC 215 - 의료 정보학(Health informatics)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~107 △1963년 TC 108~111 △1964년 TC 112~115, TC 117 △1965년 TC 118 △1966년 TC 119~122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146~150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~161 △1975년 TC 162~164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171~174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~186 △1984년 TC 188 △1985년 TC 189~191 △1988년 TC 192~194 △1989년 TC 195 △1990년 TC 197, TC 198 △1991년 TC 199, TC 201, TC 202 △1992년 TC 204~206 △1993년 TC 209 △1994년 TC 210, TC 211 △1996년 TC 213, TC 214 등이 있다.ISO/TC 215 의료 정보학(Health informatics)과 관련된 기술위원회는 1998년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는 레이첼 호손(Ms Rachel Hawthorne)가 책임지고 있다. 현재 의장은 토드 쿠퍼(Mr Todd Cooper)이며 임기는 2026년 말까지다. ISO 기술 프로그램 관리자는 마호 다카하시(Mme Maho Takahashi), ISO 편집 관리자는 발레리아 아가넨노네(Ms Valeria Agamennone) 등이다.범위는 의료 관련 데이터, 의료 시스템의 모든 측면을 지원하고 활성화하는 지식의 수집, 교환 및 사용을 촉진하기 위한 의료 정보학 분야의 표준화다.현재 ISO/TC 215 사무국과 관련해 발행된 표준은 237개며 ISO/TC 215 사무국의 직접적인 책임 하에 발행된 표준은 225개다.ISO/TC 215과 관련해 개발 중인 표준은 64개며 이중 ISO/TC 215 사무국의 직접적인 책임 하에 개발 중인 표준은 62개다. 참여하고 있는 회원은 35개국, 참관 회원은 32개국이다.□ ISO/TC 215 사무국의 직접적인 책임 하에 발행된 표준 225개 중 15개 목록▷ISO 1828:2012 Health informatics — Categorial structure for terminological systems of surgical procedures▷ISO/TR 4421:2023 Health informatics — Introduction to Ayurveda informatics▷ISO/TS 5044:2023 Health informatics — Information model for quality control of traditional Chinese medicinal products▷ISO/TS 5118:2022 Health informatics — Categorial structure of representation for evaluation of clinical practice guidelines of traditional Chinese medicine▷ISO/TS 5346:2022 Health informatics — Categorial structure for representation of traditional Chinese medicine clinical decision support system▷ISO 5477:2023 Health informatics — Interoperability of public health emergency preparedness and response information systems▷ISO/TS 5499:2024 Health informatics — Clinical particulars — Core principles for the harmonization of therapeutic indications terms and identifiers▷ISO/TS 5568:2022 Health informatics — Traditional Chinese medicine — Labelling metadata of human biological sample information▷ISO/TS 5569:2023 Health informatics — Conceptual data model for Chinese medicinal herbs▷ISO/TR 9143:2023 Health informatics — Sex and gender in electronic health records▷ISO 10159:2011 Health informatics — Messages and communication — Web access reference manifest▷ISO 10781:2023 Health informatics — HL7 Electronic Health Record-System Functional Model, Release 2.1 (EHR FM)▷ISO/IEEE 11073-00103:2015 Health informatics — Personal health device communication — Part 00103: Overview▷ISO/IEEE 11073-10101:2020 Health informatics — Device interoperability — Part 10101: Point-of-care medical device communication — Nomenclature▷ISO/IEEE 11073-10102:2014 Health informatics — Point-of-care medical device communication — Part 10102: Nomenclature — Annotated ECG□ ISO/TC 215 사무국의 직접적인 책임 하에 개발 중인 표준 62개 중 15개 목록▷ISO/AWI TR 4419 Health informatics — Reducing clinicians burden▷ISO/DTS 5384 Health informatics - Categorial Structure and Data Elements for the Identification and Exchange of Immunization Data▷ISO/CD TS 5615 Health informatics — Accelerating Safe, Effective and Secure Remote Connected Care and Mobile Health Through Standards-Based Interoperability Solutions Addressing Gaps Revealed by Pandemics▷ISO/DTS 5777 Health informatics — The architecture of internet healthcare service network▷ISO/DTS 5788 Health informatics — Internet healthcare service pattern▷ISO/CD TS 6201.2 Health Informatics — Personalized Digital Health -Framework▷ISO/CD TS 6204 Health Informatics — Categorial structures for representation of Ayurvedic medicinal water — Decocting process in Ayurveda▷ISO/AWI TS 6226 Health informatics — Reference architecture for syndromic surveillance systems for infectious diseases▷ISO/DTR 6231 Health informatics — Standardizing graphical content▷ISO/CD TS 6268-1 Health informatics — Cybersecurity framework for telehealth environments — Part 1: Overview and Concepts▷ISO/AWI TS 6268-2 Health informatics — Cybersecurity framework for telehealth environments — Part 2: Cybersecurity reference models of telehealth▷ISO/CD TS 7122 Health Informatics — Guidelines for exchanging data generated by POCT (Point of Care Testing) devices between screening center and clinical laboratory▷ISO/AWI TS 9166 Health Informatics — Guidelines for self-assessment questionnaire systems▷ISO/DTS 9320 Health informatics — Standardized data set for transfer of hemodialysis patients▷ISO/DTS 9321 Health informatics — General requirements of multi-centre medical data collaborative analysis□ ISO/TC 215 사무국 분과위원회(Subcommittee)의 책임 하에 발행 및 개발 중인 표준 현황▷ISO/TC 215/SC 1 Genomics Informatics ; 발행된 표준 12개, 개발 중인 표준 2개 -
![[특집-기술위원회] TC 212 - 의료 실험실 및 체외 진단 시스템(Medical laboratories and in vitro diagnostic systems)](http://www.stdnews.kr/data/file/news/thumb/thumb-3555376144_BhEA6wb4_51ef50f86de96bbf578dcb167daf3ff298371d44_200x180.jpg) [특집-기술위원회] TC 212 - 의료 실험실 및 체외 진단 시스템(Medical laboratories and in vitro diagnostic systems)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~107 △1963년 TC 108~111 △1964년 TC 112~115, TC 117 △1965년 TC 118 △1966년 TC 119~122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146~150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~161 △1975년 TC 162~164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171~174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~186 △1984년 TC 188 △1985년 TC 189~191 △1988년 TC 192~194 △1989년 TC 195 △1990년 TC 197, TC 198 △1991년 TC 199, TC 201, TC 202 △1992년 TC 204~206 △1993년 TC 209 등이 있다.ISO/TC 212 의료 실험실 및 체외 진단 시스템(Medical laboratories and in vitro diagnostic systems)과 관련된 기술위원회는 TC 210, TC 211과 마찬가지로 1994년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는데이비드 스테리(Mr David Sterry)가 책임지고 있다. 현재 의장은 헤수스 루에다 로드리게스(Mr Jesus Rueda Rodriguez)이며 임기는 2027년말까지다. ISO 기술 프로그램 관리자는 이사벨 베가(Ms Isabelle Vega), ISO 편집 관리자는 발레리아 아가넨노네(Ms Valeria Agamennone) 등이다.범위는 의료 실험실 및 체외 진단 시스템 분야의 표준화 및 지침이다. 여기에는 품질 관리, 분석 전후 절차, 분석 성능, 실험실 안전, 참조 시스템 및 품질 보증 등이 포함된다.단, ISO/TC 176에서 다루는 일반 품질 관리 표준, ISO/TC 210에서 다루는 의료기기 품질 관리 표준, ISO/TC 334 참조 자료 위원회(REMCO)에서 다루는 참조 자료 지침, ISO 적합성 평가 위원회(CASCO)에서 다루는 적합성 평가 지침 등은 제외된다현재 ISO/TC 212 사무국의 직접적인 책임 하에 발행된 표준은 47개며 ISO/TC 212 사무국의 직접적인 책임 하에 개발 중인 표준은 23개다. 참여하고 있는 회원은 41개국, 참관 회원은 33개국이다.□ ISO/TC 212 사무국의 직접적인 책임 하에 발행된 표준 47개 중 15개 목록▷ISO 4307:2021 Molecular in vitro diagnostic examinations — Specifications for pre-examination processes for saliva — Isolated human DNA▷ISO/TS 5798:2022 In vitro diagnostic test systems — Requirements and recommendations for detection of severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) by nucleic acid amplification methods▷ISO 15189:2022 Medical laboratories — Requirements for quality and competence▷ISO 15190:2020 Medical laboratories — Requirements for safety▷ISO 15193:2009 In vitro diagnostic medical devices — Measurement of quantities in samples of biological origin — Requirements for content and presentation of reference measurement procedures▷ISO 15194:2009 In vitro diagnostic medical devices — Measurement of quantities in samples of biological origin — Requirements for certified reference materials and the content of supporting documentation▷ISO 15195:2018 Laboratory medicine — Requirements for the competence of calibration laboratories using reference measurement procedures▷ISO 15197:2013 In vitro diagnostic test systems — Requirements for blood-glucose monitoring systems for self-testing in managing diabetes mellitus▷ISO 15198:2004 Clinical laboratory medicine — In vitro diagnostic medical devices — Validation of user quality control procedures by the manufacturer▷ISO 16256:2021 Clinical laboratory testing and in vitro diagnostic test systems — Broth micro-dilution reference method for testing the in vitro activity of antimicrobial agents against yeast fungi involved in infectious diseases▷ISO/TS 16782:2016 Clinical laboratory testing — Criteria for acceptable lots of dehydrated Mueller-Hinton agar and broth for antimicrobial susceptibility testing▷ISO 17511:2020 In vitro diagnostic medical devices — Requirements for establishing metrological traceability of values assigned to calibrators, trueness control materials and human samples▷ISO/TS 17518:2015 Medical laboratories — Reagents for staining biological material — Guidance for users▷ISO 17593:2022 Clinical laboratory testing and in vitro medical devices — Requirements for in vitro monitoring systems for self-testing of oral anticoagulant therapy▷ISO 17822:2020 In vitro diagnostic test systems — Nucleic acid amplification-based examination procedures for detection and identification of microbial pathogens — Laboratory quality practice guide□ ISO/TC 212 사무국의 직접적인 책임 하에 개발 중인 표준 23개 중 15개 목록▷ISO/DTS 5441 Competence requirements for biorisk management advisors▷ISO/DIS 5649 Medical laboratories — Concepts and specifications for the design, development, implementation, and use of laboratory-developed tests▷ISO/AWI TS 7446 ISO 35001 — Biorisk management for laboratories and other related organisations — Implementation guidance▷ISO/CD TS 7552-1 Specifications for pre-examination processes for circulating tumor cells (CTCs) in venous whole blood — Part 1: Isolated RNA▷ISO/CD TS 7552-2 Specifications for pre-examination processes for circulating tumor cells (CTCs) in venous whole blood — Part 2: Isolated DNA▷ISO/CD TS 7552-3 Specifications for pre-examination processes for circulating tumor cells (CTCs) in venous whole blood — Part 3: Preparations for analytical CTC staining▷ISO/AWI TS 8219 Sequencing and clinical application to infectious diseases▷ISO/DIS 15193 In vitro diagnostic medical devices — Requirements for reference measurement procedures▷ISO/DIS 15194 In vitro diagnostic medical devices — Requirements for certified reference materials and the content of supporting documentation▷ISO/CD TS 16766.2 Manufacturers’considerations for in vitro diagnostic medical devices in a public health crisis▷ISO/AWI TS 18701 Molecular in vitro diagnostic examinations — Specificationsfor pre-examination processes for human specimens — Isolated microbiome DNA▷ISO/AWI TS 18702 Molecular in vitro diagnostic examinations — Specifications for pre-examination processes for exosomes and other extracellular vesicles in venous whole blood — DNA, RNA and proteins▷ISO/AWI 18703 Molecular in vitro diagnostic examinations — Specifications for pre-examination processes for venous whole blood — Isolated circulating cell free RNA from plasma▷ISO/CD 18704 Molecular in vitro diagnostic examinations — Specifications for pre-examination processes for urine and other body fluids — Isolated cell free DNA▷ISO/DIS 21474-3 In vitro diagnostic medical devices — Multiplex molecular testing for nucleic acids — Part 3: Interpretation and reports
[특집-기술위원회] TC 212 - 의료 실험실 및 체외 진단 시스템(Medical laboratories and in vitro diagnostic systems)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~107 △1963년 TC 108~111 △1964년 TC 112~115, TC 117 △1965년 TC 118 △1966년 TC 119~122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146~150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~161 △1975년 TC 162~164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171~174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~186 △1984년 TC 188 △1985년 TC 189~191 △1988년 TC 192~194 △1989년 TC 195 △1990년 TC 197, TC 198 △1991년 TC 199, TC 201, TC 202 △1992년 TC 204~206 △1993년 TC 209 등이 있다.ISO/TC 212 의료 실험실 및 체외 진단 시스템(Medical laboratories and in vitro diagnostic systems)과 관련된 기술위원회는 TC 210, TC 211과 마찬가지로 1994년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는데이비드 스테리(Mr David Sterry)가 책임지고 있다. 현재 의장은 헤수스 루에다 로드리게스(Mr Jesus Rueda Rodriguez)이며 임기는 2027년말까지다. ISO 기술 프로그램 관리자는 이사벨 베가(Ms Isabelle Vega), ISO 편집 관리자는 발레리아 아가넨노네(Ms Valeria Agamennone) 등이다.범위는 의료 실험실 및 체외 진단 시스템 분야의 표준화 및 지침이다. 여기에는 품질 관리, 분석 전후 절차, 분석 성능, 실험실 안전, 참조 시스템 및 품질 보증 등이 포함된다.단, ISO/TC 176에서 다루는 일반 품질 관리 표준, ISO/TC 210에서 다루는 의료기기 품질 관리 표준, ISO/TC 334 참조 자료 위원회(REMCO)에서 다루는 참조 자료 지침, ISO 적합성 평가 위원회(CASCO)에서 다루는 적합성 평가 지침 등은 제외된다현재 ISO/TC 212 사무국의 직접적인 책임 하에 발행된 표준은 47개며 ISO/TC 212 사무국의 직접적인 책임 하에 개발 중인 표준은 23개다. 참여하고 있는 회원은 41개국, 참관 회원은 33개국이다.□ ISO/TC 212 사무국의 직접적인 책임 하에 발행된 표준 47개 중 15개 목록▷ISO 4307:2021 Molecular in vitro diagnostic examinations — Specifications for pre-examination processes for saliva — Isolated human DNA▷ISO/TS 5798:2022 In vitro diagnostic test systems — Requirements and recommendations for detection of severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) by nucleic acid amplification methods▷ISO 15189:2022 Medical laboratories — Requirements for quality and competence▷ISO 15190:2020 Medical laboratories — Requirements for safety▷ISO 15193:2009 In vitro diagnostic medical devices — Measurement of quantities in samples of biological origin — Requirements for content and presentation of reference measurement procedures▷ISO 15194:2009 In vitro diagnostic medical devices — Measurement of quantities in samples of biological origin — Requirements for certified reference materials and the content of supporting documentation▷ISO 15195:2018 Laboratory medicine — Requirements for the competence of calibration laboratories using reference measurement procedures▷ISO 15197:2013 In vitro diagnostic test systems — Requirements for blood-glucose monitoring systems for self-testing in managing diabetes mellitus▷ISO 15198:2004 Clinical laboratory medicine — In vitro diagnostic medical devices — Validation of user quality control procedures by the manufacturer▷ISO 16256:2021 Clinical laboratory testing and in vitro diagnostic test systems — Broth micro-dilution reference method for testing the in vitro activity of antimicrobial agents against yeast fungi involved in infectious diseases▷ISO/TS 16782:2016 Clinical laboratory testing — Criteria for acceptable lots of dehydrated Mueller-Hinton agar and broth for antimicrobial susceptibility testing▷ISO 17511:2020 In vitro diagnostic medical devices — Requirements for establishing metrological traceability of values assigned to calibrators, trueness control materials and human samples▷ISO/TS 17518:2015 Medical laboratories — Reagents for staining biological material — Guidance for users▷ISO 17593:2022 Clinical laboratory testing and in vitro medical devices — Requirements for in vitro monitoring systems for self-testing of oral anticoagulant therapy▷ISO 17822:2020 In vitro diagnostic test systems — Nucleic acid amplification-based examination procedures for detection and identification of microbial pathogens — Laboratory quality practice guide□ ISO/TC 212 사무국의 직접적인 책임 하에 개발 중인 표준 23개 중 15개 목록▷ISO/DTS 5441 Competence requirements for biorisk management advisors▷ISO/DIS 5649 Medical laboratories — Concepts and specifications for the design, development, implementation, and use of laboratory-developed tests▷ISO/AWI TS 7446 ISO 35001 — Biorisk management for laboratories and other related organisations — Implementation guidance▷ISO/CD TS 7552-1 Specifications for pre-examination processes for circulating tumor cells (CTCs) in venous whole blood — Part 1: Isolated RNA▷ISO/CD TS 7552-2 Specifications for pre-examination processes for circulating tumor cells (CTCs) in venous whole blood — Part 2: Isolated DNA▷ISO/CD TS 7552-3 Specifications for pre-examination processes for circulating tumor cells (CTCs) in venous whole blood — Part 3: Preparations for analytical CTC staining▷ISO/AWI TS 8219 Sequencing and clinical application to infectious diseases▷ISO/DIS 15193 In vitro diagnostic medical devices — Requirements for reference measurement procedures▷ISO/DIS 15194 In vitro diagnostic medical devices — Requirements for certified reference materials and the content of supporting documentation▷ISO/CD TS 16766.2 Manufacturers’considerations for in vitro diagnostic medical devices in a public health crisis▷ISO/AWI TS 18701 Molecular in vitro diagnostic examinations — Specificationsfor pre-examination processes for human specimens — Isolated microbiome DNA▷ISO/AWI TS 18702 Molecular in vitro diagnostic examinations — Specifications for pre-examination processes for exosomes and other extracellular vesicles in venous whole blood — DNA, RNA and proteins▷ISO/AWI 18703 Molecular in vitro diagnostic examinations — Specifications for pre-examination processes for venous whole blood — Isolated circulating cell free RNA from plasma▷ISO/CD 18704 Molecular in vitro diagnostic examinations — Specifications for pre-examination processes for urine and other body fluids — Isolated cell free DNA▷ISO/DIS 21474-3 In vitro diagnostic medical devices — Multiplex molecular testing for nucleic acids — Part 3: Interpretation and reports -
![[특집-기술위원회] TC 210 - 의료기기를 포함한 건강 목적 제품의 품질 관리 및 이에 상응하는 일반적인 측면(Quality management and corresponding general aspects for products with a health purpose including medical devices](http://www.stdnews.kr/data/file/news/thumb/thumb-3555414841_HBIn4u7g_d077e1db04057cc94b457d89772a2317beaab82c_200x180.jpg) [특집-기술위원회] TC 210 - 의료기기를 포함한 건강 목적 제품의 품질 관리 및 이에 상응하는 일반적인 측면(Quality management and corresponding general aspects for products with a health purpose including medical devices스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~107 △1963년 TC 108~111 △1964년 TC 112~115, TC 117 △1965년 TC 118 △1966년 TC 119~122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146~150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~161 △1975년 TC 162~164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171~174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~186 △1984년 TC 188 △1985년 TC 189~191 △1988년 TC 192~194 △1989년 TC 195 △1990년 TC 197, TC 198 △1991년 TC 199, TC 201, TC 202 △1992년 TC 204~206 △1993년 TC 209 등이 있다.ISO/TC 210 의료기기를 포함한 건강 목적 제품의 품질 관리 및 이에 상응하는 일반적인 측면(Quality management and corresponding general aspects for products with a health purpose including medical devices)과 관련된 기술위원회는 1994년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는 아미르 어바우탈레브(Mr Amir Aboutaleb)가 책임지고 있다. 현재 의장은 스콧 A. 콜번(Mr Scott A. Colburn)이며 임기는 2025년말까지다. ISO 기술 프로그램 관리자는 키르시 실란데르-반 후넨(Mrs Kirsi Silander-van Hunen), ISO 편집 관리자는 클라우디아 루에제(Ms Claudia Lueje) 등이다.범위는 액체 및 가스용 커넥터를 포함하는 건강 목적의 제품에 대한 품질 관리 및 상응하는 일반적인 측면과 관련한 분야의 요구 사항 및 지침에 관한 표준화다.단, △ISO/TC 176에서 다루는 일반 품질 관리 표준 △의약품 및 의료 서비스에 대한 품질 관리 표준은 제외한다.참고로 건강 목적의 제품에는 의료 기기, 인접 제품(또는 액세서리라고도 할 수 있음) 및 의료 기기와 유사한 위험 프로필을 가진 제품을 포함해 건강과 관련된 사용을 위한 제품이 포함된다.현재 ISO/TC 210 사무국의 직접적인 책임 하에 발행된 표준은 30개며 ISO/TC 210 사무국의 직접적인 책임 하에 개발 중인 표준은 13개다. 참여하고 있는 회원은 39개국, 참관 회원은 28개국이다.□ ISO/TC 210 사무국의 직접적인 책임 하에 발행된 표준 30개 중 15개 목록▷ISO 13485:2016 Medical devices — Quality management systems — Requirements for regulatory purposes▷ISO 14971:2019 Medical devices — Application of risk management to medical devices▷ISO 15223-1:2021 Medical devices — Symbols to be used with information to be supplied by the manufacturer — Part 1: General requirements▷ISO 15223-2:2010 Medical devices — Symbols to be used with medical device labels, labelling, and information to be supplied — Part 2: Symbol development, selection and validation▷ISO 18250-1:2018 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 1: General requirements and common test methods▷ISO 18250-3:2018 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 3: Enteral applications▷ISO 18250-6:2019 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 6: Neural applications▷ISO 18250-7:2018 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 7: Connectors for intravascular infusion▷ISO 18250-8:2018 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 8: Citrate-based anticoagulant solution for apheresis applications▷ISO/TR 20416:2020 Medical devices — Post-market surveillance for manufacturers▷ISO 20417:2021 Medical devices — Information to be supplied by the manufacturer▷ISO/TR 24971:2020 Medical devices — Guidance on the application of ISO 14971▷IEC 62304:2006 Medical device software — Software life cycle processes▷IEC 62304:2006/Amd 1:2015 Medical device software — Software life cycle processes — Amendment 1▷IEC 62366-1:2015 Medical devices — Part 1: Application of usability engineering to medical devices□ ISO/TC 210 사무국의 직접적인 책임 하에 개발 중인 표준 13개 목록▷ISO/WD TS 5137 Medical device maintenance management for healthcare delivery organizations▷ISO 15223-1:2021/AWI Amd 1 Medical devices — Symbols to be used with information to be supplied by the manufacturer — Part 1: General requirements — Amendment 1▷ISO/AWI 15223-2 Medical devices — Symbols to be used with medical device labels, labelling, and information to be supplied — Part 2: Symbol development, selection and validation▷ISO/AWI 18250-3 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 3: Enteral applications▷ISO 18250-8:2018/AWI Amd 1 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 8: Citrate-based anticoagulant solution for apheresis applications — Amendment 1▷ISO/CD 20417 Medical devices — Information to be supplied by the manufacturer▷ISO/AWI 23421 Medical devices — Terminology — Terms used in the field of quality management and corresponding general aspects for products with a health purpose including medical devices▷ISO/CD TS 24971-2 Medical devices — Guidance on the application of ISO 14971 — Part 2: Machine learning in artificial intelligence▷ISO/DIS 80369-1 Small-bore connectors for liquids and gases in healthcare applications — Part 1: General requirements▷ISO/FDIS 80369-2 Small-bore connectors for liquids and gases in healthcare applications — Part 2: Connectors for respiratory applications▷IEC/AWI 80369-5 Small-bore connectors for liquids and gases in healthcare applications — Part 5: Connectors for limb cuff inflation applications▷ISO/DIS 80369-6 Small bore connectors for liquids and gases in healthcare applications — Part 6: Connectors for neural applications▷ISO/FDIS 80369-20 Small-bore connectors for liquids and gases in healthcare applications — Part 20: Common test methods
[특집-기술위원회] TC 210 - 의료기기를 포함한 건강 목적 제품의 품질 관리 및 이에 상응하는 일반적인 측면(Quality management and corresponding general aspects for products with a health purpose including medical devices스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~107 △1963년 TC 108~111 △1964년 TC 112~115, TC 117 △1965년 TC 118 △1966년 TC 119~122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146~150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~161 △1975년 TC 162~164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171~174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~186 △1984년 TC 188 △1985년 TC 189~191 △1988년 TC 192~194 △1989년 TC 195 △1990년 TC 197, TC 198 △1991년 TC 199, TC 201, TC 202 △1992년 TC 204~206 △1993년 TC 209 등이 있다.ISO/TC 210 의료기기를 포함한 건강 목적 제품의 품질 관리 및 이에 상응하는 일반적인 측면(Quality management and corresponding general aspects for products with a health purpose including medical devices)과 관련된 기술위원회는 1994년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는 아미르 어바우탈레브(Mr Amir Aboutaleb)가 책임지고 있다. 현재 의장은 스콧 A. 콜번(Mr Scott A. Colburn)이며 임기는 2025년말까지다. ISO 기술 프로그램 관리자는 키르시 실란데르-반 후넨(Mrs Kirsi Silander-van Hunen), ISO 편집 관리자는 클라우디아 루에제(Ms Claudia Lueje) 등이다.범위는 액체 및 가스용 커넥터를 포함하는 건강 목적의 제품에 대한 품질 관리 및 상응하는 일반적인 측면과 관련한 분야의 요구 사항 및 지침에 관한 표준화다.단, △ISO/TC 176에서 다루는 일반 품질 관리 표준 △의약품 및 의료 서비스에 대한 품질 관리 표준은 제외한다.참고로 건강 목적의 제품에는 의료 기기, 인접 제품(또는 액세서리라고도 할 수 있음) 및 의료 기기와 유사한 위험 프로필을 가진 제품을 포함해 건강과 관련된 사용을 위한 제품이 포함된다.현재 ISO/TC 210 사무국의 직접적인 책임 하에 발행된 표준은 30개며 ISO/TC 210 사무국의 직접적인 책임 하에 개발 중인 표준은 13개다. 참여하고 있는 회원은 39개국, 참관 회원은 28개국이다.□ ISO/TC 210 사무국의 직접적인 책임 하에 발행된 표준 30개 중 15개 목록▷ISO 13485:2016 Medical devices — Quality management systems — Requirements for regulatory purposes▷ISO 14971:2019 Medical devices — Application of risk management to medical devices▷ISO 15223-1:2021 Medical devices — Symbols to be used with information to be supplied by the manufacturer — Part 1: General requirements▷ISO 15223-2:2010 Medical devices — Symbols to be used with medical device labels, labelling, and information to be supplied — Part 2: Symbol development, selection and validation▷ISO 18250-1:2018 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 1: General requirements and common test methods▷ISO 18250-3:2018 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 3: Enteral applications▷ISO 18250-6:2019 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 6: Neural applications▷ISO 18250-7:2018 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 7: Connectors for intravascular infusion▷ISO 18250-8:2018 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 8: Citrate-based anticoagulant solution for apheresis applications▷ISO/TR 20416:2020 Medical devices — Post-market surveillance for manufacturers▷ISO 20417:2021 Medical devices — Information to be supplied by the manufacturer▷ISO/TR 24971:2020 Medical devices — Guidance on the application of ISO 14971▷IEC 62304:2006 Medical device software — Software life cycle processes▷IEC 62304:2006/Amd 1:2015 Medical device software — Software life cycle processes — Amendment 1▷IEC 62366-1:2015 Medical devices — Part 1: Application of usability engineering to medical devices□ ISO/TC 210 사무국의 직접적인 책임 하에 개발 중인 표준 13개 목록▷ISO/WD TS 5137 Medical device maintenance management for healthcare delivery organizations▷ISO 15223-1:2021/AWI Amd 1 Medical devices — Symbols to be used with information to be supplied by the manufacturer — Part 1: General requirements — Amendment 1▷ISO/AWI 15223-2 Medical devices — Symbols to be used with medical device labels, labelling, and information to be supplied — Part 2: Symbol development, selection and validation▷ISO/AWI 18250-3 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 3: Enteral applications▷ISO 18250-8:2018/AWI Amd 1 Medical devices — Connectors for reservoir delivery systems for healthcare applications — Part 8: Citrate-based anticoagulant solution for apheresis applications — Amendment 1▷ISO/CD 20417 Medical devices — Information to be supplied by the manufacturer▷ISO/AWI 23421 Medical devices — Terminology — Terms used in the field of quality management and corresponding general aspects for products with a health purpose including medical devices▷ISO/CD TS 24971-2 Medical devices — Guidance on the application of ISO 14971 — Part 2: Machine learning in artificial intelligence▷ISO/DIS 80369-1 Small-bore connectors for liquids and gases in healthcare applications — Part 1: General requirements▷ISO/FDIS 80369-2 Small-bore connectors for liquids and gases in healthcare applications — Part 2: Connectors for respiratory applications▷IEC/AWI 80369-5 Small-bore connectors for liquids and gases in healthcare applications — Part 5: Connectors for limb cuff inflation applications▷ISO/DIS 80369-6 Small bore connectors for liquids and gases in healthcare applications — Part 6: Connectors for neural applications▷ISO/FDIS 80369-20 Small-bore connectors for liquids and gases in healthcare applications — Part 20: Common test methods -
 식약처-싱가포르 보건과학청, 의약품 상호인정협정 체결식품의약품안전처는 싱가포르 보건과학청과 대한민국-싱가포르 간 의약품 제조소에 대한 제조·품질관리기준(GMP) 실태조사 결과를 상호인정하는 ‘의약품GMP 상호인정협정(MRA)’을 26일 체결했으며 이번 협정은 5월부터 공식 발효될 예정이라고 밝혔다. 싱가포르 보건과학청(Health Sciences Authority, HSA)은 싱가포르의 의약품, 의료기기 등 의료제품 인허가 및 안전관리를 담당하는 정부 부처다. 이날 오유경 식품의약품안전처장과 미미 총 보건과학청장은 양국을 대표해 한-싱가포르 FTA 분야별 부속서에 ‘의약품 GMP’를 추가하기 위한 교환각서에서명했으며 향후 한-싱가포르 양국은 상대국 정부가 실시한 의약품 GMP 적합 평가 결과를 자국에서도 동등하게 인정하기로 했다. 이에 따라 국내 기업들은 싱가포르에 의약품을 수출할 때 식약처가 발급한 GMP 적합판정서를 그대로 인정받아 허가 기간이 단축되고 그에 따른 비용이 절감되는 효과를 얻는다. 싱가포르는 태평양과 인도양이 만나는 지리적 위치, 우수한 연구 인력 등 높은 잠재력을 토대로 많은 다국적 제약사가 아시아 시장 진출을 위해 거점으로 삼고 있는아시아 지역 내 의약품 GMP 분야 선진 국가다. 식약처 관계자는 “이번 협정이 우리나라 GMP 관리체계가 국제적으로 인정받는 계기가 되고, 아세안 국가 대상 의약품 수출 기회 확대와 아세안내 다른 국가와 상호인정협정의 발판으로 작용할 것으로 기대한다”며 “앞으로도 우리나라 제약 업체가 아세안 지역 등 해외로 진출하는데 적극 지원할 계획”이라고 전했다.
식약처-싱가포르 보건과학청, 의약품 상호인정협정 체결식품의약품안전처는 싱가포르 보건과학청과 대한민국-싱가포르 간 의약품 제조소에 대한 제조·품질관리기준(GMP) 실태조사 결과를 상호인정하는 ‘의약품GMP 상호인정협정(MRA)’을 26일 체결했으며 이번 협정은 5월부터 공식 발효될 예정이라고 밝혔다. 싱가포르 보건과학청(Health Sciences Authority, HSA)은 싱가포르의 의약품, 의료기기 등 의료제품 인허가 및 안전관리를 담당하는 정부 부처다. 이날 오유경 식품의약품안전처장과 미미 총 보건과학청장은 양국을 대표해 한-싱가포르 FTA 분야별 부속서에 ‘의약품 GMP’를 추가하기 위한 교환각서에서명했으며 향후 한-싱가포르 양국은 상대국 정부가 실시한 의약품 GMP 적합 평가 결과를 자국에서도 동등하게 인정하기로 했다. 이에 따라 국내 기업들은 싱가포르에 의약품을 수출할 때 식약처가 발급한 GMP 적합판정서를 그대로 인정받아 허가 기간이 단축되고 그에 따른 비용이 절감되는 효과를 얻는다. 싱가포르는 태평양과 인도양이 만나는 지리적 위치, 우수한 연구 인력 등 높은 잠재력을 토대로 많은 다국적 제약사가 아시아 시장 진출을 위해 거점으로 삼고 있는아시아 지역 내 의약품 GMP 분야 선진 국가다. 식약처 관계자는 “이번 협정이 우리나라 GMP 관리체계가 국제적으로 인정받는 계기가 되고, 아세안 국가 대상 의약품 수출 기회 확대와 아세안내 다른 국가와 상호인정협정의 발판으로 작용할 것으로 기대한다”며 “앞으로도 우리나라 제약 업체가 아세안 지역 등 해외로 진출하는데 적극 지원할 계획”이라고 전했다. -
![[특집-기술위원회] TC 198 - 보건 의료 제품의 멸균(Sterilization of health care products)](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_2BoG0P7X_a0e507b4052a7f3b37d893ad86a6c6caa79da3d8_200x180.jpg) [특집-기술위원회] TC 198 - 보건 의료 제품의 멸균(Sterilization of health care products)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~TC 107 △1963년 TC 108~TC 111 △1964년 TC 112~TC 115, TC 117 △1965년 TC 118 △1966년 TC 119~TC 122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146, TC 147, TC 148, TC 149, TC 150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~TC 161 △1975년 TC 162~TC 164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171, TC 172, TC 173, TC 174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~TC 186 △1984년 TC 188 △1985년 TC 189, TC 190, TC 191 △1988년 TC 192~TC 194 △1989년 TC 195 등이 있다.ISO/TC 198 보건 의료 제품의 멸균(Sterilization of health care products)과 관련된 기술위원회는 TC 197과 마찬가지로 1990년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는 아만다 베네딕(Ms Amanda Benedict)가 책임지고 있다. 현재 의장은 리차드 밴크로프트(Mr Richard Bancroft)이며 임기는 2025년 말까지다.ISO 기술 프로그램 관리자는 페트리샤 쿡(Mme Patricia Cook), ISO 편집 관리자는 클라우디아 루에제(Ms Claudia Lueje)등이다. 범위는 보건의료 제품의 멸균을 위한 프로세스 및 장비의 표준화다.현재 ISO/TC 198 사무국의 직접적인 책임 하에 발행된 표준은 69개며 ISO/TC 198 사무국의 직접적인 책임 하에 개발 중인 표준은 15개다. 참여하고 있는 회원은 34개국, 참관 회원은 21개국이다.□ ISO/TC 198 사무국의 직접적인 책임 하에 발행된 표준 69개 중 15개 목록▷ISO/TS 5111:2022 Guidance on quality of water for sterilizers, sterilization and washer-disinfectors for health care products▷ISO 11135:2014 Sterilization of health-care products — Ethylene oxide — Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO 11135:2014/Amd 1:2018 Sterilization of health-care products — Ethylene oxide — Requirements for the development, validation and routine control of a sterilization process for medical devices — Amendment 1: Revision of Annex E, Single batch release▷ISO 11137-1:2006 Sterilization of health care products — Radiation — Part 1: Requirements for development, validation and routine control of a sterilization process for medical devices▷ISO 11137-1:2006/Amd 1:2013 Sterilization of health care products — Radiation — Part 1: Requirements for development, validation and routine control of a sterilization process for medical devices — Amendment 1▷ISO 11137-1:2006/Amd 2:2018 Sterilization of health care products — Radiation — Part 1: Requirements for development, validation and routine control of a sterilization process for medical devices — Amendment 2: Revision to 4.3.4 and 11.2▷ISO 11137-2:2013 Sterilization of health care products — Radiation — Part 2: Establishing the sterilization dose▷ISO 11137-2:2013/Amd 1:2022 Sterilization of health care products — Radiation — Part 2: Establishing the sterilization dose — Amendment 1▷ISO 11137-3:2017 Sterilization of health care products — Radiation — Part 3: Guidance on dosimetric aspects of development, validation and routine control▷ISO/TS 11137-4:2020 Sterilization of health care products — Radiation — Part 4: Guidance on process control▷ISO 11138-1:2017 Sterilization of health care products — Biological indicators — Part 1: General requirements▷ISO 11138-2:2017 Sterilization of health care products — Biological indicators — Part 2: Biological indicators for ethylene oxide sterilization processes▷ISO 11138-3:2017 Sterilization of health care products — Biological indicators — Part 3: Biological indicators for moist heat sterilization processes▷ISO 11138-4:2017 Sterilization of health care products — Biological indicators — Part 4: Biological indicators for dry heat sterilization processes▷ISO 11138-5:2017 Sterilization of health care products — Biological indicators — Part 5: Biological indicators for low-temperature steam and formaldehyde sterilization processes□ ISO/TC 198 사무국의 직접적인 책임 하에 개발 중인 표준 15개 목록▷ISO/DIS 11135.2 Sterilization of health care products — Ethylene oxide — Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO/FDIS 11137-1 Sterilization of health care products — Radiation — Part 1: Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO/CD 11140-3 Sterilization of health care products — Chemical indicators — Part 3: Class 2 indicator systems for use in the Bowie and Dick-type steam penetration test▷ISO/CD 11140-4 Sterilization of health care products — Chemical indicators — Part 4: Class 2 indicators as an alternative to the Bowie and Dick-type test for detection of steam penetration▷ISO/CD 11140-5 Sterilization of health care products — Chemical indicators — Part 5: Class 2 indicators for Bowie and Dick-type air removal tests▷ISO/AWI 11607-3 Packaging for terminally sterilized medical devices — Part 3: Requirements for process development for forming, sealing and assembly▷ISO/AWI 11737-1 Sterilization of health care products — Microbiological methods — Part 1: Determination of a population of microorganisms on products▷ISO/FDIS 15883-1 Washer-disinfectors — Part 1: General requirements, terms and definitions and tests▷ISO/DIS 15883-2 Washer-disinfectors — Part 2: Requirements and tests for washer-disinfectors employing thermal disinfection for critical and semi-critical medical devices▷ISO/DIS 15883-3 Washer-disinfectors — Part 3: Requirements and tests for washer-disinfectors employing thermal disinfection for human waste containers▷ISO/CD 15883-6 Washer-disinfectors — Part 6: Requirements and tests for washer-disinfectors employing thermal disinfection for noncritical medical devices and health care equipment▷ISO/DIS 15883-7 Washer-disinfectors — Part 7: Requirements and tests for washer-disinfectors employing chemical disinfection for non-critical thermolabile medical devices and health care equipment▷ISO/AWI TS 17664-3 Processing of health care products — Information to be provided by the medical device manufacturer for the processing of medical devices — Part 3: Guidance on the designation of a reusable medical device to a quantitative cleaning classification▷ISO 17665 Sterilization of health care products — Moist heat — Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO/AWI 19253 Sterilization of health care products — Application of ISO/TS 22421 to the requirements for sterilizers used for the terminal sterilization of health care products containing aqueous liquid in sealed containers
[특집-기술위원회] TC 198 - 보건 의료 제품의 멸균(Sterilization of health care products)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~TC 107 △1963년 TC 108~TC 111 △1964년 TC 112~TC 115, TC 117 △1965년 TC 118 △1966년 TC 119~TC 122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146, TC 147, TC 148, TC 149, TC 150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~TC 161 △1975년 TC 162~TC 164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171, TC 172, TC 173, TC 174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~TC 186 △1984년 TC 188 △1985년 TC 189, TC 190, TC 191 △1988년 TC 192~TC 194 △1989년 TC 195 등이 있다.ISO/TC 198 보건 의료 제품의 멸균(Sterilization of health care products)과 관련된 기술위원회는 TC 197과 마찬가지로 1990년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는 아만다 베네딕(Ms Amanda Benedict)가 책임지고 있다. 현재 의장은 리차드 밴크로프트(Mr Richard Bancroft)이며 임기는 2025년 말까지다.ISO 기술 프로그램 관리자는 페트리샤 쿡(Mme Patricia Cook), ISO 편집 관리자는 클라우디아 루에제(Ms Claudia Lueje)등이다. 범위는 보건의료 제품의 멸균을 위한 프로세스 및 장비의 표준화다.현재 ISO/TC 198 사무국의 직접적인 책임 하에 발행된 표준은 69개며 ISO/TC 198 사무국의 직접적인 책임 하에 개발 중인 표준은 15개다. 참여하고 있는 회원은 34개국, 참관 회원은 21개국이다.□ ISO/TC 198 사무국의 직접적인 책임 하에 발행된 표준 69개 중 15개 목록▷ISO/TS 5111:2022 Guidance on quality of water for sterilizers, sterilization and washer-disinfectors for health care products▷ISO 11135:2014 Sterilization of health-care products — Ethylene oxide — Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO 11135:2014/Amd 1:2018 Sterilization of health-care products — Ethylene oxide — Requirements for the development, validation and routine control of a sterilization process for medical devices — Amendment 1: Revision of Annex E, Single batch release▷ISO 11137-1:2006 Sterilization of health care products — Radiation — Part 1: Requirements for development, validation and routine control of a sterilization process for medical devices▷ISO 11137-1:2006/Amd 1:2013 Sterilization of health care products — Radiation — Part 1: Requirements for development, validation and routine control of a sterilization process for medical devices — Amendment 1▷ISO 11137-1:2006/Amd 2:2018 Sterilization of health care products — Radiation — Part 1: Requirements for development, validation and routine control of a sterilization process for medical devices — Amendment 2: Revision to 4.3.4 and 11.2▷ISO 11137-2:2013 Sterilization of health care products — Radiation — Part 2: Establishing the sterilization dose▷ISO 11137-2:2013/Amd 1:2022 Sterilization of health care products — Radiation — Part 2: Establishing the sterilization dose — Amendment 1▷ISO 11137-3:2017 Sterilization of health care products — Radiation — Part 3: Guidance on dosimetric aspects of development, validation and routine control▷ISO/TS 11137-4:2020 Sterilization of health care products — Radiation — Part 4: Guidance on process control▷ISO 11138-1:2017 Sterilization of health care products — Biological indicators — Part 1: General requirements▷ISO 11138-2:2017 Sterilization of health care products — Biological indicators — Part 2: Biological indicators for ethylene oxide sterilization processes▷ISO 11138-3:2017 Sterilization of health care products — Biological indicators — Part 3: Biological indicators for moist heat sterilization processes▷ISO 11138-4:2017 Sterilization of health care products — Biological indicators — Part 4: Biological indicators for dry heat sterilization processes▷ISO 11138-5:2017 Sterilization of health care products — Biological indicators — Part 5: Biological indicators for low-temperature steam and formaldehyde sterilization processes□ ISO/TC 198 사무국의 직접적인 책임 하에 개발 중인 표준 15개 목록▷ISO/DIS 11135.2 Sterilization of health care products — Ethylene oxide — Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO/FDIS 11137-1 Sterilization of health care products — Radiation — Part 1: Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO/CD 11140-3 Sterilization of health care products — Chemical indicators — Part 3: Class 2 indicator systems for use in the Bowie and Dick-type steam penetration test▷ISO/CD 11140-4 Sterilization of health care products — Chemical indicators — Part 4: Class 2 indicators as an alternative to the Bowie and Dick-type test for detection of steam penetration▷ISO/CD 11140-5 Sterilization of health care products — Chemical indicators — Part 5: Class 2 indicators for Bowie and Dick-type air removal tests▷ISO/AWI 11607-3 Packaging for terminally sterilized medical devices — Part 3: Requirements for process development for forming, sealing and assembly▷ISO/AWI 11737-1 Sterilization of health care products — Microbiological methods — Part 1: Determination of a population of microorganisms on products▷ISO/FDIS 15883-1 Washer-disinfectors — Part 1: General requirements, terms and definitions and tests▷ISO/DIS 15883-2 Washer-disinfectors — Part 2: Requirements and tests for washer-disinfectors employing thermal disinfection for critical and semi-critical medical devices▷ISO/DIS 15883-3 Washer-disinfectors — Part 3: Requirements and tests for washer-disinfectors employing thermal disinfection for human waste containers▷ISO/CD 15883-6 Washer-disinfectors — Part 6: Requirements and tests for washer-disinfectors employing thermal disinfection for noncritical medical devices and health care equipment▷ISO/DIS 15883-7 Washer-disinfectors — Part 7: Requirements and tests for washer-disinfectors employing chemical disinfection for non-critical thermolabile medical devices and health care equipment▷ISO/AWI TS 17664-3 Processing of health care products — Information to be provided by the medical device manufacturer for the processing of medical devices — Part 3: Guidance on the designation of a reusable medical device to a quantitative cleaning classification▷ISO 17665 Sterilization of health care products — Moist heat — Requirements for the development, validation and routine control of a sterilization process for medical devices▷ISO/AWI 19253 Sterilization of health care products — Application of ISO/TS 22421 to the requirements for sterilizers used for the terminal sterilization of health care products containing aqueous liquid in sealed containers -
 식약처, ‘첨단 동물대체시험법 표준화 국제심포지엄’ 개최식품의약품안전처 소속 식품의약품안전평가원은 첨단 동물대체시험 연구와 정책 동향을 공유하고 동물대체시험 표준화 인프라를 구축하기 위해 22일 서울 중구 신라호텔에서 ‘첨단 동물대체시험법 표준화 국제심포지엄’을 개최한다고 밝혔다. 이번 국제심포지엄이 첨단 바이오 기술 기반 동물대체시험 표준화에 도움이 될 것으로 기대된다. 이번 국제심포지엄에서는 ▲미국 FDA, NIEHS 첨단 동물대체시험 개발 현황 및 규제적용 ▲OECD 첨단 동물대체시험 활용 및 전망 ▲OECD 첨단 동물대체시험 기반 가이드라인 및 추진 프로젝트 소개 ▲한국동물대체시험검증센터(KoCVAM) 및 국내 동물대체시험 규제적용 등에 대한 전문가 발표가 있을 예정이다. NIEHS(National Institute of Environmental Health Science)는 첨단 동물대체시험 연구 및 인체·환경 보건 등을 담당하는 미국 규제기관이다. 관심 있는 누구나 사전등록(https://naver.me/xSNH1Djj) 후 이번 국제심포지엄에 참석할 수 있으며 사전등록은 16일까지 가능하다. 식약처 관계자는 “이번 국제심포지엄이 오가노이드 등 첨단 바이오 기술 기반 동물대체시험 표준화에 도움을 줄 것으로 기대한다”며 “앞으로도 산업계, 학계, 관련 부처 등의 다양한 의견을 청취하고 협력하는 등 국내 동물대체시험 분야 연구 개발을 적극 지원할 계획”이라고 밝혔다.
식약처, ‘첨단 동물대체시험법 표준화 국제심포지엄’ 개최식품의약품안전처 소속 식품의약품안전평가원은 첨단 동물대체시험 연구와 정책 동향을 공유하고 동물대체시험 표준화 인프라를 구축하기 위해 22일 서울 중구 신라호텔에서 ‘첨단 동물대체시험법 표준화 국제심포지엄’을 개최한다고 밝혔다. 이번 국제심포지엄이 첨단 바이오 기술 기반 동물대체시험 표준화에 도움이 될 것으로 기대된다. 이번 국제심포지엄에서는 ▲미국 FDA, NIEHS 첨단 동물대체시험 개발 현황 및 규제적용 ▲OECD 첨단 동물대체시험 활용 및 전망 ▲OECD 첨단 동물대체시험 기반 가이드라인 및 추진 프로젝트 소개 ▲한국동물대체시험검증센터(KoCVAM) 및 국내 동물대체시험 규제적용 등에 대한 전문가 발표가 있을 예정이다. NIEHS(National Institute of Environmental Health Science)는 첨단 동물대체시험 연구 및 인체·환경 보건 등을 담당하는 미국 규제기관이다. 관심 있는 누구나 사전등록(https://naver.me/xSNH1Djj) 후 이번 국제심포지엄에 참석할 수 있으며 사전등록은 16일까지 가능하다. 식약처 관계자는 “이번 국제심포지엄이 오가노이드 등 첨단 바이오 기술 기반 동물대체시험 표준화에 도움을 줄 것으로 기대한다”며 “앞으로도 산업계, 학계, 관련 부처 등의 다양한 의견을 청취하고 협력하는 등 국내 동물대체시험 분야 연구 개발을 적극 지원할 계획”이라고 밝혔다. -
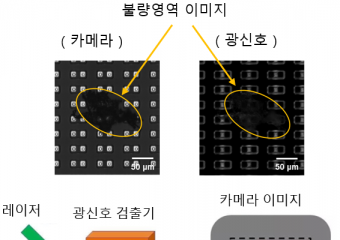
 KRISS, 배관 누출 사고 막는 ‘지하매설 파손 예방 기술’ 개발한국표준과학연구원(KRISS, 원장 박현민)이 무단 굴착 등으로 발생하는 배관 누출 사고를 사전에 예방할 수 있는 지하 매설 배관 파손 예방 및 조기 탐지 시스템을 개발했다. 이번 기술의 보급으로 국민 안전과 사회적 비용 절감 실현에 더욱 가까워질 전망이다. 무단 굴착공사는 물, 석유, 가스 등을 수송하는 지하 매설 배관의 주요 파손 원인 중 하나로, 배관 관리주체에서 사전에 파악하기 어렵다. 파손으로 누출사고 발생 시 환경오염은 물론 폭발, 화재, 싱크홀 등의 위험이 따르지만 예방적 관리가 힘든 것은 이런 이유에서다. KRISS 구조안전모니터링팀이 개발한 이번 기술은 지하 매설 배관이 파손되기 전에 외부 손상 요인을 실시간 탐지해 사고를 방지하는 시스템이다. 무단 굴착공사 등으로 배관에 충격이 가해지면 이를 파손 위험 징후로 포착해 조기 경보한다. 기술의 핵심은 배관 충격 시 배관을 통해 전파되는 탄성파의 정밀측정 센서와 분석 알고리즘이다. 배관에 수백 미터 간격으로 한 쌍의 센서를 부착하면 두 센서 사이에서 발생하는 충격 신호를 실시간 모니터링해 충격이 발생한 시각과 위치 정보를 즉각 산출할 수 있다. 지진 관측센터에서 진동을 감지한 후 지진파의 도달 속도를 이용해 지진의 발생 시각과 위치를 계산하는 것과 같은 원리다. 해당 센서는 별도의 굴착공사 없이 밸브실이나 맨홀 등 기존 매설 배관의 외부 노출 부분에 간단히 부착해 설치할 수 있다. 주위 교통환경으로 인한 소음 등 불필요한 신호를 저감하고 배관에서 발생한 신호만 판별하는 정확한 분석 알고리즘도 갖췄다. 연구진은 청주, 전주, 오송 등 세 곳의 테스트베드를 운영해 수 km에 이르는 실사용 매설 배관에서 이번 시스템의 현장 적용성을 검증했다. 실험 결과 해당 시스템은 배관에 가해지는 약 20 kN(킬로뉴턴) 이상의 충격을 95% 이상의 정확도로 감지해냈다. 배관 파손을 일으키는 충격의 강도는 통상 약 수백 kN 이상으로, 이번 성과가 배관 파손사고 예방 및 조기 경보에 적합함이 확인됐다. 기존의 매설 배관 건전성 모니터링 기술은 대부분 배관 파손으로 인한 누출 탐지에 초점을 맞췄다. 장거리 배관의 파손 위험을 사전 감지하는 시스템이 개발된 것은 이번이 세계 최초다. 해당 성과는 올해 국내 기업에 기술이전을 마쳤으며 미국, 유럽에도 특허 출원됐다. 이번 성과는 상수도뿐 아니라 송유, 가스, 열공급 등 다양한 분야의 배관에 적용 가능하다. 매설 배관의 이상 상태를 온라인으로 사전 감지·조치하기 위한 스마트 감시시스템에 활용될 수 있다. 환경부 물관리연구사업과 KRISS 기본사업, 과학기술정보통신부 연구개발특구육성사업의 지원을 받은 이번 연구의 성과는 올해 8월 스트럭처럴 헬스 모니터링(Structural Health Monitoring, IF: 6.6) 게재를 포함해 지금까지 4건의 국제학술지에 게재됐다.
KRISS, 배관 누출 사고 막는 ‘지하매설 파손 예방 기술’ 개발한국표준과학연구원(KRISS, 원장 박현민)이 무단 굴착 등으로 발생하는 배관 누출 사고를 사전에 예방할 수 있는 지하 매설 배관 파손 예방 및 조기 탐지 시스템을 개발했다. 이번 기술의 보급으로 국민 안전과 사회적 비용 절감 실현에 더욱 가까워질 전망이다. 무단 굴착공사는 물, 석유, 가스 등을 수송하는 지하 매설 배관의 주요 파손 원인 중 하나로, 배관 관리주체에서 사전에 파악하기 어렵다. 파손으로 누출사고 발생 시 환경오염은 물론 폭발, 화재, 싱크홀 등의 위험이 따르지만 예방적 관리가 힘든 것은 이런 이유에서다. KRISS 구조안전모니터링팀이 개발한 이번 기술은 지하 매설 배관이 파손되기 전에 외부 손상 요인을 실시간 탐지해 사고를 방지하는 시스템이다. 무단 굴착공사 등으로 배관에 충격이 가해지면 이를 파손 위험 징후로 포착해 조기 경보한다. 기술의 핵심은 배관 충격 시 배관을 통해 전파되는 탄성파의 정밀측정 센서와 분석 알고리즘이다. 배관에 수백 미터 간격으로 한 쌍의 센서를 부착하면 두 센서 사이에서 발생하는 충격 신호를 실시간 모니터링해 충격이 발생한 시각과 위치 정보를 즉각 산출할 수 있다. 지진 관측센터에서 진동을 감지한 후 지진파의 도달 속도를 이용해 지진의 발생 시각과 위치를 계산하는 것과 같은 원리다. 해당 센서는 별도의 굴착공사 없이 밸브실이나 맨홀 등 기존 매설 배관의 외부 노출 부분에 간단히 부착해 설치할 수 있다. 주위 교통환경으로 인한 소음 등 불필요한 신호를 저감하고 배관에서 발생한 신호만 판별하는 정확한 분석 알고리즘도 갖췄다. 연구진은 청주, 전주, 오송 등 세 곳의 테스트베드를 운영해 수 km에 이르는 실사용 매설 배관에서 이번 시스템의 현장 적용성을 검증했다. 실험 결과 해당 시스템은 배관에 가해지는 약 20 kN(킬로뉴턴) 이상의 충격을 95% 이상의 정확도로 감지해냈다. 배관 파손을 일으키는 충격의 강도는 통상 약 수백 kN 이상으로, 이번 성과가 배관 파손사고 예방 및 조기 경보에 적합함이 확인됐다. 기존의 매설 배관 건전성 모니터링 기술은 대부분 배관 파손으로 인한 누출 탐지에 초점을 맞췄다. 장거리 배관의 파손 위험을 사전 감지하는 시스템이 개발된 것은 이번이 세계 최초다. 해당 성과는 올해 국내 기업에 기술이전을 마쳤으며 미국, 유럽에도 특허 출원됐다. 이번 성과는 상수도뿐 아니라 송유, 가스, 열공급 등 다양한 분야의 배관에 적용 가능하다. 매설 배관의 이상 상태를 온라인으로 사전 감지·조치하기 위한 스마트 감시시스템에 활용될 수 있다. 환경부 물관리연구사업과 KRISS 기본사업, 과학기술정보통신부 연구개발특구육성사업의 지원을 받은 이번 연구의 성과는 올해 8월 스트럭처럴 헬스 모니터링(Structural Health Monitoring, IF: 6.6) 게재를 포함해 지금까지 4건의 국제학술지에 게재됐다. -
![[특집-ISO/IEC JTC 1/SC 17 활동] ⑧Liaison document from CEN/CLC JTC 13: Cyber Security and Data Protection presentation 소개](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374351_2EiqtloM_de337de45aa1ce7f1807f72af981ad9b11a1b49a_200x180.jpg) [특집-ISO/IEC JTC 1/SC 17 활동] ⑧Liaison document from CEN/CLC JTC 13: Cyber Security and Data Protection presentation 소개지난 10월16일 ISO/IEC 공동기술위원회 산하 분과위원회 SC 17은 'Liaison document from CEN/CLC JTC 13: Cyber Security and Data Protection presentation' 관련 문서를 배포했다.ISO/IEC JTC 1/SC 17 카드 및 개인 식별을 위한 보안 장치(Cards and security devices for personal identification)는 국제표준화기구(ISO와 국제전기기술위원회(IEC)의 공동 기술 위원회(JTC) ISO/IEC JTC 1의 표준화 분과위원회다.ISO/IEC JTC 1/SC 17의 국제사무국은 영국에 위치한 영국표준협회(BSI)이며 신분증 및 개인 식별 분야 표준을 개발하고 촉진하는 역할을 담당하고 있다.배포된 문서는 'Liaison document from CEN/CLC JTC 13: Cyber Security and Data Protection presentation는 10월9일 생성된 문서의 네번째 수정판(v.0.4)이다.유럽표준화기구(European Standardization Organizations) CEN/CLC/JTC 13 사이버보안 및 데이터 보호(Cyber Security and Data Protection)에 대한 문서다.개요(Overview)는 1. General, 2. Scope, 3. Structure, 4. Working Groups, 5. Further Information 등으로 구성됐다. 1. General 파트는 다음과 같이 구성됐다.△CEN/CLC/JTC 13 Cybersecurity and Data Protection - Joint Technical Committee (JTC) of CEN and CENELEC - established November 2017△120+ European experts on Cybersecurity and Data Protection△7 dedicated Working Groups△3 Plenary Meetings/Sessions per Year△Annual Outreach Events△Chairperson: Walter Fumy, Bundesdruckerei (Germany)△Secretariat: DIN German Institute of Standardization (Germany)△Secretary: Martin Uhlherr (DIN)△CEN-CENELEC Management Centre Program Manager: Laurens Hernalsteen 2. Scope 파트는 다음과 같다.△Development of horizontal Standards in the Field of Cybersecurity and Data Protection for vertical Applications Domains△Horizontal Security & Privacy Topics of the evolving interconnected Society, driven by the European Market in Domains such as ICT, eHealth, Transport, Smart Cities, Automotive, IOT△Key Issues - Management Systems, Frameworks, Methodologies - Data Protection and Privacy - Services and Products Evaluation Standards suitable for Security Assessment for large Companies and small and medium Enterprises - Competence Requirements for Cybersecurity and Data Protection - Security Requirements, Services, Techniques and Guidelines for ICT Systems, Services, Networks and Devices, including Smart Objects and distributed Computing Devices△Identification and Adoption of published Documents by ISO/IEC JTC 1, other SDOs, international Bodies and industrial Fora△Development of CEN/CENELEC Publications for safeguarding Information - 이하 생략 -
[특집-ISO/IEC JTC 1/SC 17 활동] ⑧Liaison document from CEN/CLC JTC 13: Cyber Security and Data Protection presentation 소개지난 10월16일 ISO/IEC 공동기술위원회 산하 분과위원회 SC 17은 'Liaison document from CEN/CLC JTC 13: Cyber Security and Data Protection presentation' 관련 문서를 배포했다.ISO/IEC JTC 1/SC 17 카드 및 개인 식별을 위한 보안 장치(Cards and security devices for personal identification)는 국제표준화기구(ISO와 국제전기기술위원회(IEC)의 공동 기술 위원회(JTC) ISO/IEC JTC 1의 표준화 분과위원회다.ISO/IEC JTC 1/SC 17의 국제사무국은 영국에 위치한 영국표준협회(BSI)이며 신분증 및 개인 식별 분야 표준을 개발하고 촉진하는 역할을 담당하고 있다.배포된 문서는 'Liaison document from CEN/CLC JTC 13: Cyber Security and Data Protection presentation는 10월9일 생성된 문서의 네번째 수정판(v.0.4)이다.유럽표준화기구(European Standardization Organizations) CEN/CLC/JTC 13 사이버보안 및 데이터 보호(Cyber Security and Data Protection)에 대한 문서다.개요(Overview)는 1. General, 2. Scope, 3. Structure, 4. Working Groups, 5. Further Information 등으로 구성됐다. 1. General 파트는 다음과 같이 구성됐다.△CEN/CLC/JTC 13 Cybersecurity and Data Protection - Joint Technical Committee (JTC) of CEN and CENELEC - established November 2017△120+ European experts on Cybersecurity and Data Protection△7 dedicated Working Groups△3 Plenary Meetings/Sessions per Year△Annual Outreach Events△Chairperson: Walter Fumy, Bundesdruckerei (Germany)△Secretariat: DIN German Institute of Standardization (Germany)△Secretary: Martin Uhlherr (DIN)△CEN-CENELEC Management Centre Program Manager: Laurens Hernalsteen 2. Scope 파트는 다음과 같다.△Development of horizontal Standards in the Field of Cybersecurity and Data Protection for vertical Applications Domains△Horizontal Security & Privacy Topics of the evolving interconnected Society, driven by the European Market in Domains such as ICT, eHealth, Transport, Smart Cities, Automotive, IOT△Key Issues - Management Systems, Frameworks, Methodologies - Data Protection and Privacy - Services and Products Evaluation Standards suitable for Security Assessment for large Companies and small and medium Enterprises - Competence Requirements for Cybersecurity and Data Protection - Security Requirements, Services, Techniques and Guidelines for ICT Systems, Services, Networks and Devices, including Smart Objects and distributed Computing Devices△Identification and Adoption of published Documents by ISO/IEC JTC 1, other SDOs, international Bodies and industrial Fora△Development of CEN/CENELEC Publications for safeguarding Information - 이하 생략 - -
![[특집-공동기술위원회] ①JTC 1, 정보 기술(Information technology)](http://www.stdnews.kr/img/no_image_282_80.png) [특집-공동기술위원회] ①JTC 1, 정보 기술(Information technology)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC1~TC323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(Working Group, WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등을 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.또한 국제전기기술위원회(International Electro-technical Commission, IEC)는 전기 및 전자 제품의 고품질 인프라와 국제 무역을 뒷받침하는 글로벌 비영리 회원 조직이다. 기술 혁신, 저렴한 인프라 개발, 효율적이고 지속 가능한 에너지 접근, 스마트 도시화 및 교통 시스템, 기후 변화 완화를 촉진하고 사람과 환경의 안전을 향상시키는 역할을 수행하고 있다. 170개 이상의 국가를 통합하고 전 세계 2만명의 전문가에게 글로벌, 중립적이며 독립적인 표준화 플랫폼을 제공하고 있다. 장치, 시스템, 설치, 서비스 및 인력이 필요에 따라 작동함을 구성원이 인증하는 4가지 적합성 평가 시스템을 관리한다.적합성 평가와 함께 정부가 국가 품질 인프라를 구축하고 모든 규모의 기업이 전 세계 대부분의 국가에서 일관되게 안전하고 신뢰할 수 있는 제품을 사고 팔 수 있도록 하는 기술 프레임워크를 제공하는 약 1만개의 IEC 국제표준을 발행하고 있다.이러한 ISO와 IEC가 공동으로 구성한 기술위원회 ISO/IEC JTC 1 정보 기술(Information technology)에 대해 살펴볼 예정이다. JTC 1은 1987년 결성됐으며 사무국은 미국국립표준협회(American National Standards Institute, ANSI)에서 맡고 있다. 위원회는 리사 라지첼(Mrs Lisa Rajchel)가 책임지고 있다. 현재 의장은 필 웬블롬(Mr Phil Wennblom)으로 임기는 202년까지다.ISO 기술 프로그램 관리자는 앤드류 드라이든(Mr Andrew Dryden), 스티븐 더트널(Mr Stephen Dutnall), ISO 편집 관리자는 앨리슨 레이드 자몬드(Ms Alison Reid-Jamond) 등으로 조사됐다. 범위는 정보기술 분야의 표준화다.현재 ISO/IEC JTC 1의 직접적인 책임 하에 발행된 표준은 517개며 직접적인 책임하에 개발 중인 표준은 23개다. 참여하고 있는 회원은 40개국, 참관 회원은 62개국이다.□ ISO/IEC JTC 1 사무국의 직접적인 책임 하에 발행된 표준 517개 중 15개 목록▷ISO 1538:1984 Programming languages — ALGOL 60▷ISO 1730:1980 Dictation equipment — Basic operating requirements▷ISO 1858:1977 Information processing — General purpose hubs and reels, with 76 mm (3 in) centrehole, for magnetic tape used in interchange instrumentation applications▷ISO 1859:1973 Information processing — Unrecorded magnetic tapes for interchange instrumentation applications — General dimensional requirements▷ISO 1860:1986 Information processing — Precision reels for magnetic tape used in interchange instrumentation applications▷ISO 2257:1980 Office machines and printing machines used for information processing — Widths of fabric printing ribbons on spools▷ISO 2258:1976 Printing ribbons — Minimum markings to appear on containers▷ISO/IEC 2382:2015 Information technology — Vocabulary▷ISO 2775:1977 Office machines and printing machines used for information processing — Widths of one-time paper or plastic printing ribbons and marking to indicate the end of the ribbons▷ISO 2784:1974 Continuous forms used for information processing — Sizes and sprocket feed holes▷ISO/IEC 3532-1:2023 Information technology — Medical image-based modelling for 3D printing — Part 1: General requirements▷ISO 3540:1976 Paper or plastic printing ribbons — Characteristics of cores▷ISO 3791:1976 Office machines and data processing equipment — Keyboard layouts for numeric applications▷ISO 3792:1976 Adding machines — Layout of function keyboard▷ISO 3802:1976 Information processing — General purpose reels with 8 mm (5/16 in) centre hole for magnetic tape for interchange instrumentation applications□ ISO/IEC JTC 1 사무국의 직접적인 책임 하에 개발중인 표준 23개 중 15개 목록▷ISO/IEC FDIS 3532-2 Information technology — Medical image-based modelling for 3D printing — Part 2: Segmentation▷ISO/IEC DIS 4879 Information technology — Quantum computing — Terminology and vocabulary▷ISO/IEC DIS 5087-2 Information technology — City data model — Part 2: City level concepts▷ISO/IEC DIS 5153-1 Information Technology — City service platform for public health emergencies — Part 1: Overview and general requirements▷ISO/IEC AWI 8801 Information Technology — 3D Printing and Scanning-- 3D scanned and labeled data Standard Operating Procedure (SOP) for evaluation of modelling from 3D scanned data▷ISO/IEC AWI 8803 Information Technology — 3D Printing and Scanning — accuracy and precision evaluation process for modeling from 3D scanned data▷ISO/IEC DIS 14776-346 Information technology — Small computer system interface (SCSI) — Part 346: Zoned Block Commands - 2 (ZBC-2)▷ISO/IEC AWI 16466 Information Technology — 3D Printing and scanning — Assessment methods of 3D scanned data for 3D printing model▷ISO/IEC DIS 17760-105 Information technology — ATA Command Set - 5 (ACS-5) — Part 105: Title missing▷ISO/IEC DIS 17917 Smart cities — Guidance to establishing a decision-making framework for sharing data and information services▷ISO/IEC AWI TR 18157 Information technology — Introduction to quantum computing▷ISO/IEC PRF 18974 Information technology — OpenChain security assurance specificationISO/IEC DIS 19987 Information technology — EPC Information Services (EPCIS)▷ISO/IEC DIS 19988 Information technology — Core Business Vocabulary (CBV)▷ISO/IEC AWI TR 20169 Information technology — Overview of smart city standardization
[특집-공동기술위원회] ①JTC 1, 정보 기술(Information technology)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC1~TC323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(Working Group, WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등을 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.또한 국제전기기술위원회(International Electro-technical Commission, IEC)는 전기 및 전자 제품의 고품질 인프라와 국제 무역을 뒷받침하는 글로벌 비영리 회원 조직이다. 기술 혁신, 저렴한 인프라 개발, 효율적이고 지속 가능한 에너지 접근, 스마트 도시화 및 교통 시스템, 기후 변화 완화를 촉진하고 사람과 환경의 안전을 향상시키는 역할을 수행하고 있다. 170개 이상의 국가를 통합하고 전 세계 2만명의 전문가에게 글로벌, 중립적이며 독립적인 표준화 플랫폼을 제공하고 있다. 장치, 시스템, 설치, 서비스 및 인력이 필요에 따라 작동함을 구성원이 인증하는 4가지 적합성 평가 시스템을 관리한다.적합성 평가와 함께 정부가 국가 품질 인프라를 구축하고 모든 규모의 기업이 전 세계 대부분의 국가에서 일관되게 안전하고 신뢰할 수 있는 제품을 사고 팔 수 있도록 하는 기술 프레임워크를 제공하는 약 1만개의 IEC 국제표준을 발행하고 있다.이러한 ISO와 IEC가 공동으로 구성한 기술위원회 ISO/IEC JTC 1 정보 기술(Information technology)에 대해 살펴볼 예정이다. JTC 1은 1987년 결성됐으며 사무국은 미국국립표준협회(American National Standards Institute, ANSI)에서 맡고 있다. 위원회는 리사 라지첼(Mrs Lisa Rajchel)가 책임지고 있다. 현재 의장은 필 웬블롬(Mr Phil Wennblom)으로 임기는 202년까지다.ISO 기술 프로그램 관리자는 앤드류 드라이든(Mr Andrew Dryden), 스티븐 더트널(Mr Stephen Dutnall), ISO 편집 관리자는 앨리슨 레이드 자몬드(Ms Alison Reid-Jamond) 등으로 조사됐다. 범위는 정보기술 분야의 표준화다.현재 ISO/IEC JTC 1의 직접적인 책임 하에 발행된 표준은 517개며 직접적인 책임하에 개발 중인 표준은 23개다. 참여하고 있는 회원은 40개국, 참관 회원은 62개국이다.□ ISO/IEC JTC 1 사무국의 직접적인 책임 하에 발행된 표준 517개 중 15개 목록▷ISO 1538:1984 Programming languages — ALGOL 60▷ISO 1730:1980 Dictation equipment — Basic operating requirements▷ISO 1858:1977 Information processing — General purpose hubs and reels, with 76 mm (3 in) centrehole, for magnetic tape used in interchange instrumentation applications▷ISO 1859:1973 Information processing — Unrecorded magnetic tapes for interchange instrumentation applications — General dimensional requirements▷ISO 1860:1986 Information processing — Precision reels for magnetic tape used in interchange instrumentation applications▷ISO 2257:1980 Office machines and printing machines used for information processing — Widths of fabric printing ribbons on spools▷ISO 2258:1976 Printing ribbons — Minimum markings to appear on containers▷ISO/IEC 2382:2015 Information technology — Vocabulary▷ISO 2775:1977 Office machines and printing machines used for information processing — Widths of one-time paper or plastic printing ribbons and marking to indicate the end of the ribbons▷ISO 2784:1974 Continuous forms used for information processing — Sizes and sprocket feed holes▷ISO/IEC 3532-1:2023 Information technology — Medical image-based modelling for 3D printing — Part 1: General requirements▷ISO 3540:1976 Paper or plastic printing ribbons — Characteristics of cores▷ISO 3791:1976 Office machines and data processing equipment — Keyboard layouts for numeric applications▷ISO 3792:1976 Adding machines — Layout of function keyboard▷ISO 3802:1976 Information processing — General purpose reels with 8 mm (5/16 in) centre hole for magnetic tape for interchange instrumentation applications□ ISO/IEC JTC 1 사무국의 직접적인 책임 하에 개발중인 표준 23개 중 15개 목록▷ISO/IEC FDIS 3532-2 Information technology — Medical image-based modelling for 3D printing — Part 2: Segmentation▷ISO/IEC DIS 4879 Information technology — Quantum computing — Terminology and vocabulary▷ISO/IEC DIS 5087-2 Information technology — City data model — Part 2: City level concepts▷ISO/IEC DIS 5153-1 Information Technology — City service platform for public health emergencies — Part 1: Overview and general requirements▷ISO/IEC AWI 8801 Information Technology — 3D Printing and Scanning-- 3D scanned and labeled data Standard Operating Procedure (SOP) for evaluation of modelling from 3D scanned data▷ISO/IEC AWI 8803 Information Technology — 3D Printing and Scanning — accuracy and precision evaluation process for modeling from 3D scanned data▷ISO/IEC DIS 14776-346 Information technology — Small computer system interface (SCSI) — Part 346: Zoned Block Commands - 2 (ZBC-2)▷ISO/IEC AWI 16466 Information Technology — 3D Printing and scanning — Assessment methods of 3D scanned data for 3D printing model▷ISO/IEC DIS 17760-105 Information technology — ATA Command Set - 5 (ACS-5) — Part 105: Title missing▷ISO/IEC DIS 17917 Smart cities — Guidance to establishing a decision-making framework for sharing data and information services▷ISO/IEC AWI TR 18157 Information technology — Introduction to quantum computing▷ISO/IEC PRF 18974 Information technology — OpenChain security assurance specificationISO/IEC DIS 19987 Information technology — EPC Information Services (EPCIS)▷ISO/IEC DIS 19988 Information technology — Core Business Vocabulary (CBV)▷ISO/IEC AWI TR 20169 Information technology — Overview of smart city standardization -
![[기획-디지털 ID 표준] ⑤유럽표준화기구(ESOs) 및 표준 - 소속 기술위원회(TC)](http://www.stdnews.kr/data/file/news/thumb/thumb-3555376253_R18lsJHo_0a6c5e577e0958e7d463fa5c1e4139d855b26ed2_200x180.jpg) [기획-디지털 ID 표준] ⑤유럽표준화기구(ESOs) 및 표준 - 소속 기술위원회(TC)디지털 ID(Digital Identity) 분야에서 상호운용(interoperable)이 가능하고 안전한 서비스 보장을 위한 표준에 대한 수요가 증가하고 있다. 다양한 표준 조직 및 산업 기관이 활동하는 이유다. 유럽표준화기구(European Standardisation Organistions, ESOs), 유럽표준화위원회(European Committee for Standardization, CEN), 유럽전기기술표준화위원회(European Committee for Electrotechnical Standardization, CENELEC), 유럽전기통신표준화기구(European Telecommunication Standards Institute, ETSI) 등 디지털 ID 관련 표준을 개발하고 있는 기술위원회에 대해 살펴보면 다음과 같다.먼저 유럽전기통신표준화기구(ETSI)는 유럽의 eIDAS 규정과 전자 거래에 대한 신뢰를 제공하기 위한 국제사회의 일반 요구사항을 지원하는 다수의 표준을 발표했다.특히 ETSI 전자 서명 및 인프라 기술위원회(ETSI Electronic Signatures and Infrastructures Technical Committee)는 서비스 제공업체를 위한 정책, 보안 및 기술 요구사항에 대한 여러 표준을 제정했다.기술위원회(ETSI ESI/TC)는 디지털 서명의 형식, 생성, 검증을 위한 절차, 정책, 신뢰 앵커로서 신뢰할 수 있는 목록을 다룬다.CEN 기술위원회 224(CEN Technical Committee 224, CEN/TC 224)-MACHINE-READABLE CARDS, RELATED DEVICE INTERFACES AND OPERATIONS는 다중 부문 환경에서 보안 요소, 시스템, 운영, 개인정보 보호를 갖는 개인 식별 및 관련 개인 장치와 관련이 있다.기술위원회는 개인 식별, 관련 개인 장치의 상호운용성, 보안을 강화하기 위한 여러 표준을 발표했다. 이 중 CEN 기술위원회 224 내 워킹그룹 17, 18, 19이 디지털 ID와 관련이 있다.다른 실무그룹(Working Group, WG)은 WG 17 : ‘Protection Profiles in the Context of SSCD(secure signature creation device)’ △WG 18 : ‘Biometrics’ △WG 19 : ‘Breeder Documents' 등이다. 최근 유럽 디지털 지갑 EUDI Wallet 표준을 개발하기 위해 WG 20이 임시로 구성됐다.CEN/TC 224는 다중 부문 환경에서 개인 식별 및 관련 개인 장치, 시스템, 운영 및 개인 정보 보호의 상호 운용성과 보안을 강화하기 위해 표준을 개발하고 있다.여기에는 전자 식별, 전자 서명, 지불 및 청구, 출입, 국경 통제와 같은 애플리케이션 및 서비스와 같은 작업을 포함하고 있다. 또한 △카드, 모바일 장치 및 관련 인터페이스와 같이 폼 팩터와 독립적인 보안 요소를 갖춘 개인 장치 △인증, 기밀성, 무결성, 생체 인식, 개인 데이터 및 민감한 데이터 보호를 포함한 보안 서비스 △수용 장치, 서버, 암호화 모듈과 같은 시스템 구성 요소 등도 해당된다.CEN/TC 224 다중 부문 환경은 정부·시민, 교통, 은행, 전자 보건과 같은 부문 뿐만 아니라 카드 제조업체, 보안 기술, 적합성 평가기관, 소프트웨어 제조업체와 같은 공급 측면의 소비자 및 공급자가 포함된다. 참고로 CEN 기술 위원회 224 내 실무 그룹(WG)은 다음과 같다.▷CEN/TC 224/WG 1 - ICC physical characteristics▷CEN/TC 224/WG 2 - General concepts for ICC systems▷CEN/TC 224/WG 3 - Device interface characteristics▷CEN/TC 224/WG 6 - User Interface▷CEN/TC 224/WG 7 - PIN presentation▷CEN/TC 224/WG 8 - Thin flexible cards▷CEN/TC 224/WG 9 - Telecommunication applications▷CEN/TC 224/WG 10 - Intersector electronic purse▷CEN/TC 224/WG 11 - Transport applications▷CEN/TC 224/WG 12 - Health applications▷CEN/TC 224/WG 15 - European citizen card▷CEN/TC 224/WG 16 - Application Interface for smart cards used as Secure Signature Creation Devices▷CEN/TC 224/WG 17 - Protection Profiles in the context of SSCD▷CEN/TC 224/WG 18 - Interoperability of biometric recorded data▷CEN/TC 224/WG 19 - Breeder Documents▷CEN/TC 224/WG 20 - Ad Hoc Group on European Digital Identity WalletsCEN/CENELEC 공동 기술위원회 19(CEN/CENELEC Joint Technical Committee 19)는 블록체인(Blockchain) 및 분산 원장 기술(Distributed Ledger Technologies)을 다루는 위원회다.특히 실무 그룹 1(Working Group 1) : 분산형 신원 관리(Decentralised Identity Management)는 ISO 카운터파트너 ISO 기술위원회 307( ISO Technical Committee 307)과 긴밀한 접촉을 유지하고 있다.분산형 ID 관리(decentralised identity management) 및 DLTs(Distributed Ledger Technologies)에 의해 제공되는 지원 기능을 위한 프로세스, 역할, 관행에 대한 것이다. 식별자, 키, 증거 레지스트리, 트러스트 앵커(trust anchors) 관리를 포함한다.실무그룹 2(WG 2)는 환경 지속가능성(CEN/CLC/JTC 19/WG 2 - Environmental sustainability)을 다루고 있다.
[기획-디지털 ID 표준] ⑤유럽표준화기구(ESOs) 및 표준 - 소속 기술위원회(TC)디지털 ID(Digital Identity) 분야에서 상호운용(interoperable)이 가능하고 안전한 서비스 보장을 위한 표준에 대한 수요가 증가하고 있다. 다양한 표준 조직 및 산업 기관이 활동하는 이유다. 유럽표준화기구(European Standardisation Organistions, ESOs), 유럽표준화위원회(European Committee for Standardization, CEN), 유럽전기기술표준화위원회(European Committee for Electrotechnical Standardization, CENELEC), 유럽전기통신표준화기구(European Telecommunication Standards Institute, ETSI) 등 디지털 ID 관련 표준을 개발하고 있는 기술위원회에 대해 살펴보면 다음과 같다.먼저 유럽전기통신표준화기구(ETSI)는 유럽의 eIDAS 규정과 전자 거래에 대한 신뢰를 제공하기 위한 국제사회의 일반 요구사항을 지원하는 다수의 표준을 발표했다.특히 ETSI 전자 서명 및 인프라 기술위원회(ETSI Electronic Signatures and Infrastructures Technical Committee)는 서비스 제공업체를 위한 정책, 보안 및 기술 요구사항에 대한 여러 표준을 제정했다.기술위원회(ETSI ESI/TC)는 디지털 서명의 형식, 생성, 검증을 위한 절차, 정책, 신뢰 앵커로서 신뢰할 수 있는 목록을 다룬다.CEN 기술위원회 224(CEN Technical Committee 224, CEN/TC 224)-MACHINE-READABLE CARDS, RELATED DEVICE INTERFACES AND OPERATIONS는 다중 부문 환경에서 보안 요소, 시스템, 운영, 개인정보 보호를 갖는 개인 식별 및 관련 개인 장치와 관련이 있다.기술위원회는 개인 식별, 관련 개인 장치의 상호운용성, 보안을 강화하기 위한 여러 표준을 발표했다. 이 중 CEN 기술위원회 224 내 워킹그룹 17, 18, 19이 디지털 ID와 관련이 있다.다른 실무그룹(Working Group, WG)은 WG 17 : ‘Protection Profiles in the Context of SSCD(secure signature creation device)’ △WG 18 : ‘Biometrics’ △WG 19 : ‘Breeder Documents' 등이다. 최근 유럽 디지털 지갑 EUDI Wallet 표준을 개발하기 위해 WG 20이 임시로 구성됐다.CEN/TC 224는 다중 부문 환경에서 개인 식별 및 관련 개인 장치, 시스템, 운영 및 개인 정보 보호의 상호 운용성과 보안을 강화하기 위해 표준을 개발하고 있다.여기에는 전자 식별, 전자 서명, 지불 및 청구, 출입, 국경 통제와 같은 애플리케이션 및 서비스와 같은 작업을 포함하고 있다. 또한 △카드, 모바일 장치 및 관련 인터페이스와 같이 폼 팩터와 독립적인 보안 요소를 갖춘 개인 장치 △인증, 기밀성, 무결성, 생체 인식, 개인 데이터 및 민감한 데이터 보호를 포함한 보안 서비스 △수용 장치, 서버, 암호화 모듈과 같은 시스템 구성 요소 등도 해당된다.CEN/TC 224 다중 부문 환경은 정부·시민, 교통, 은행, 전자 보건과 같은 부문 뿐만 아니라 카드 제조업체, 보안 기술, 적합성 평가기관, 소프트웨어 제조업체와 같은 공급 측면의 소비자 및 공급자가 포함된다. 참고로 CEN 기술 위원회 224 내 실무 그룹(WG)은 다음과 같다.▷CEN/TC 224/WG 1 - ICC physical characteristics▷CEN/TC 224/WG 2 - General concepts for ICC systems▷CEN/TC 224/WG 3 - Device interface characteristics▷CEN/TC 224/WG 6 - User Interface▷CEN/TC 224/WG 7 - PIN presentation▷CEN/TC 224/WG 8 - Thin flexible cards▷CEN/TC 224/WG 9 - Telecommunication applications▷CEN/TC 224/WG 10 - Intersector electronic purse▷CEN/TC 224/WG 11 - Transport applications▷CEN/TC 224/WG 12 - Health applications▷CEN/TC 224/WG 15 - European citizen card▷CEN/TC 224/WG 16 - Application Interface for smart cards used as Secure Signature Creation Devices▷CEN/TC 224/WG 17 - Protection Profiles in the context of SSCD▷CEN/TC 224/WG 18 - Interoperability of biometric recorded data▷CEN/TC 224/WG 19 - Breeder Documents▷CEN/TC 224/WG 20 - Ad Hoc Group on European Digital Identity WalletsCEN/CENELEC 공동 기술위원회 19(CEN/CENELEC Joint Technical Committee 19)는 블록체인(Blockchain) 및 분산 원장 기술(Distributed Ledger Technologies)을 다루는 위원회다.특히 실무 그룹 1(Working Group 1) : 분산형 신원 관리(Decentralised Identity Management)는 ISO 카운터파트너 ISO 기술위원회 307( ISO Technical Committee 307)과 긴밀한 접촉을 유지하고 있다.분산형 ID 관리(decentralised identity management) 및 DLTs(Distributed Ledger Technologies)에 의해 제공되는 지원 기능을 위한 프로세스, 역할, 관행에 대한 것이다. 식별자, 키, 증거 레지스트리, 트러스트 앵커(trust anchors) 관리를 포함한다.실무그룹 2(WG 2)는 환경 지속가능성(CEN/CLC/JTC 19/WG 2 - Environmental sustainability)을 다루고 있다.




![[특집-기술위원회] TC 225 시장, 여론 및 사회 조사(Market, opinion and social research)](http://www.stdnews.kr/theme/wide03/img/default/no_img.gif)
![[특집-기술위원회] TC 224 식수, 폐수, 빗물 시스템 및 서비스(Drinking water, wastewater and](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_IlG5QH4m_135eda611f5c0ab4f936820013cfcf208ea141f0_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 35. Result of voting on SR Ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-3555379571_4cufp2BH_756bcefa64e6169e58646ad7b061ecbec455fb11_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 34. Result of voting on SR ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-3555380113_kIQxAlfN_727cc6e35ccb9d5e6c07574a3b3a2ab9db104d48_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 33. Result of voting on SR ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_R52GPIij_2bca2660198a937d2534db7bfd9fc8174a76cfa2_340x240.jpg)


![[일본] 요코하마(横浜), 3월 원격근무로 일하는 50대 여성이 장시간 노동을 강요받아 적응장애가 발병해 산재로 인정받아](http://www.stdnews.kr/data/file/news/thumb/thumb-3555377672_BapV2SmF_41a011a26290be1daa3f6a5220df7b8b6d167f69_340x240.jpg)
![[인도] 마하라슈트라주 식품의약국(Maharashtra FDA), 맥도날드 상품명에 치즈를 잘못 표기해 소비자 기만 지적](http://www.stdnews.kr/data/file/news/thumb/thumb-3743818281_Uu5GpcKZ_6890f33f4b087f58686ed20e46a04bbb79ad883e_340x240.jpg)
![[남아공] 토코만 푸드(Thokoman Foods), 자사 땅콩버터 식품 안전성 재확인](http://www.stdnews.kr/data/file/news/thumb/thumb-3743818281_h5HrK0kT_c2453abdb4577a16b34590f5b8f76de9c2a95469_340x240.jpg)
![[일본] 정부, 전국 약 1800개의 지방자치단체가 사용하는 정보기술(IT) 시스템을 공통화할 계획](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_k57HcuaC_ec1c1c40ab22bacb5547865a845790615e059a71_340x240.jpg)
![[일본] 소비자청(消費者庁), 5월 중 기능성 표시 식품 관련 제도를 전면 재검토할 계획](http://www.stdnews.kr/data/file/news/thumb/thumb-3698770111_kxPwWpEb_40955dfb17799431ea435609be9619c5595c5eac_340x240.jpg)
![[일본] 경제산업성(経済産業省), 2030년 차세대자동차인 'SDV(Software Defined Vehicle)'의 글로벌](http://www.stdnews.kr/data/file/news/thumb/thumb-3555378102_ebVNjTcg_b332bb36ad71a61dff859ea6e106c3f9cfc0e9d1_340x240.jpg)
![[일본] 혼다(ホンダ), 2030년까지 전기자동차(EV)를 중심으로 하는 전동화와 소트프웨어 개발에 10조 엔을 투자할 계획](http://www.stdnews.kr/data/file/news/thumb/thumb-3555381172_1g5z7YDN_4db7699b271b5e9dbbe1a4f6dc69fb01a9881abb_340x240.jpg)
![[일본] 자민당(自民党), 기업이 직원을 고객의 '카스하라(カスハラ)로부터 보호를 의무로 하는 방안을 고려 중](http://www.stdnews.kr/data/file/news/thumb/thumb-3555381172_PCNyaL1v_9f9b79d526b4be07024401e874fe26f618a42e7c_340x240.jpg)
![[특집-기상기후재난] 한국중부발전(주) 신정철 선임 인터뷰 - 행정안전부 뿐 아니라 기상기후 연계조직 모두가 참여하는 협의체가](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374516_iKWwUBas_9c1729f1e3977ee50c398986e7f98d5002a57deb_340x240.jpg)
![[특집-기상기후재난] (주)비밍코어 정성민 대표 인터뷰 - 인공지능(AI) 활용한 기후재난 대처 솔루션 개발](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374391_0JZYhIcj_dca23c54fc7923952082a9d7af92db00b9dd33c9_340x240.jpg)
![[기획-표준 전문가] 한국투자증권 김범수 FC 인터뷰 - 표준전문가 양성 교육이 지속되길 희망](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374114_Np9hM7aC_e6ffa916aade15e1c301badf3132ed3f0551a900_340x240.jpg)
![[특집-기상기후재난] 행정안전부 안전교육 전문인력 유정희 강사 인터뷰 - 기상기후재난예방 전문가 양성 시급](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374240_gOmdLG10_cfc17ed887dccc93f503013bf794ed568a5d40dc_340x240.jpg)
![[특집-기상기후재난] (주)이토스 김형식 대표 인터뷰 - 재난을 사전에 예측·예방할 기술개발 시급](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_lmUrCBIn_797dc8926bb7d90542546463cc73e6233f0bbb46_340x240.png)